2022-2023学年江苏省高一(下)期末化学迎考试卷
发布:2024/8/22 0:0:1
一、单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项符合题意。
-
1.硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环境问题也日益受到关注。下列说法正确的是( )
组卷:603引用:14难度:0.7 -
2.青铜剑表面的蓝色薄锈主要成分为碱式碳酸铜,其生成反应为2Cu+CO2+H2O+O2═Cu2(OH)2CO3。下列有关说法正确的是( )
组卷:40引用:1难度:0.7 -
3.乙烯可用于脱除烟气中SO2并回收单质硫,发生的反应:CH2=CH2+3SO2
3S+2CO2+2H2O。下列有关说法正确的是( )Fe2O3/CeO2△组卷:53引用:3难度:0.7 -
4.下列氮及其化合物的性质与用途的对应关系正确的是( )
组卷:107引用:1难度:0.7 -
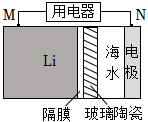 5.海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如图。下列说法错误的是( )组卷:854引用:6难度:0.6
5.海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如图。下列说法错误的是( )组卷:854引用:6难度:0.6
二、非选择题:共4题,共计61分。
-
16.氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:
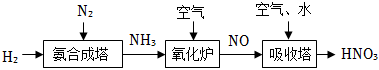
(1)下列有关NH3的说法中,不正确的是(填字母)。
A.工业合成NH3需要在高温、高压、催化剂下进行
B.NH3可用来生产碳铵和尿素等化肥
C.NH3可用浓硫酸或无水氯化钙干燥
D.NH3受热易分解,须置于冷暗处保存
(2)NH3易溶于水,标准状况下,用充满NH3的烧瓶做喷泉实验(如图),引发喷泉的方法是。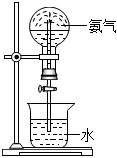
(3)氨气在氧化炉中发生反应的化学方程式为。
(4)工厂生产出的浓硝酸可用铝槽车或铁槽车来运输,是因为在常温下,浓硝酸能使铝、铁等发生现象,说明浓硝酸具有很强的性。
(5)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的污染,可用以下两种方法处理:
①可用ClO2将氮氧化物转化成。向含ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为NO-3。
②氨转化法。已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为。组卷:108引用:1难度:0.7 -
17.环境保护是化学的重要任务,请完成下列问题。
(1)采用“联合脱硫脱氮技术”处理烟气(含CO2、SO2、NO)可获得含CaCO3、CaSO4、Ca(NO2)2的副产品,工业流程如图1所示。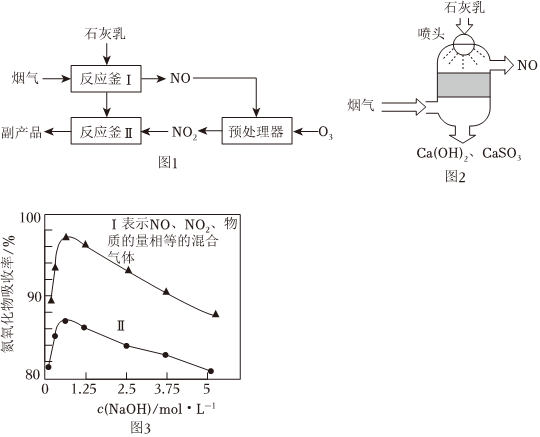
①反应釜Ⅰ采用“气—液逆流”接触吸收法(如图2),其优点是。
②反应釜Ⅱ中CaSO3转化为CaSO4反应的化学方程式为。
(2)烟气(主要污染物SO2、NOx)对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。
①烟气经O3预处理后用碱液吸收,可减少其中SO2、NOx的含量。已知NO可被O3氧化为NO2、,用NaOH溶液吸收若只生成一种盐,该盐的化学式为NO-3。
②尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为。
(3)工业上氮的氧化物通常是用碱性溶液吸收。
①用Na2CO3溶液吸收硝酸工业尾气中的NO2,生成等物质的量的两种钠盐(其中一种为NaNO2)及一种气体,反应的离子方程式为。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收NO2(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图3所示,曲线Ⅱ表示NO的物质的量(填“大于”“小于”或“等于”)NO2物质的量。当NaOH溶液浓度高于0.5mol⋅L-1后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是。组卷:96引用:1难度:0.6


