环境保护是化学的重要任务,请完成下列问题。
(1)采用“联合脱硫脱氮技术”处理烟气(含CO2、SO2、NO)可获得含CaCO3、CaSO4、Ca(NO2)2的副产品,工业流程如图1所示。
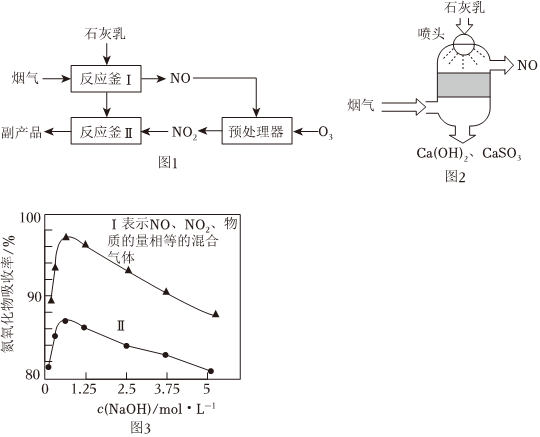
①反应釜Ⅰ采用“气—液逆流”接触吸收法(如图2),其优点是 气液接触更加充分,反应更加完全气液接触更加充分,反应更加完全。
②反应釜Ⅱ中CaSO3转化为CaSO4反应的化学方程式为 2NO2+CaSO3+Ca(OH)2═CaSO4+Ca(NO2)2+H2O2NO2+CaSO3+Ca(OH)2═CaSO4+Ca(NO2)2+H2O。
(2)烟气(主要污染物SO2、NOx)对人类生活环境造成很大的污染。工业上采取氧化、还原等方法将之除去,以达到净化目的。
①烟气经O3预处理后用碱液吸收,可减少其中SO2、NOx的含量。已知NO可被O3氧化为NO2、NO-3,用NaOH溶液吸收若只生成一种盐,该盐的化学式为 NaNO3NaNO3。
②尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为 2CO(NH2)2+6NO 高温 5N2+2CO2+4H2O2CO(NH2)2+6NO 高温 5N2+2CO2+4H2O。
(3)工业上氮的氧化物通常是用碱性溶液吸收。
①用Na2CO3溶液吸收硝酸工业尾气中的NO2,生成等物质的量的两种钠盐(其中一种为NaNO2)及一种气体,反应的离子方程式为 2NO2+CO2-3=NO-2+NO-3+CO22NO2+CO2-3=NO-2+NO-3+CO2。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收NO2(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图3所示,曲线Ⅱ表示NO的物质的量 大于大于(填“大于”“小于”或“等于”)NO2物质的量。当NaOH溶液浓度高于0.5mol⋅L-1后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是 NaOH溶液浓度越大黏稠度越高,对氮氧化物的吸收率下降NaOH溶液浓度越大黏稠度越高,对氮氧化物的吸收率下降。
N
O
-
3
高温
高温
CO
2
-
3
NO
-
2
NO
-
3
CO
2
-
3
NO
-
2
NO
-
3
【答案】气液接触更加充分,反应更加完全;2NO2+CaSO3+Ca(OH)2═CaSO4+Ca(NO2)2+H2O;NaNO3;2CO(NH2)2+6NO 5N2+2CO2+4H2O;2NO2+=++CO2;大于;NaOH溶液浓度越大黏稠度越高,对氮氧化物的吸收率下降
高温
CO
2
-
3
NO
-
2
NO
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/22 0:0:1组卷:96引用:1难度:0.6
相似题
-
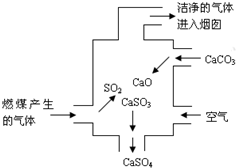 1.右图是某燃煤发电厂处理废气的装置示意图.装置内发生的主要反应中不含( )发布:2024/12/30 4:0:1组卷:331引用:16难度:0.9
1.右图是某燃煤发电厂处理废气的装置示意图.装置内发生的主要反应中不含( )发布:2024/12/30 4:0:1组卷:331引用:16难度:0.9 -
2.下列说法不正确的是( )
发布:2024/12/30 5:30:2组卷:27引用:2难度:0.9 -
3.工业上常用微生物法、吸收法、电解法、还原法等消除硫、氮等引起的污染。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生CH3COOH、H2等物质,可将废水中还原为H2S,同时用N2或CO2将H2S从水中吹出,再用碱液吸收。SO2-4
①的空间构型为SO2-4.
②CH3COOH与在SBR细菌作用下生成CO2和H2S的离子方程式为SO2-4.
③将H2S从水中吹出时,用CO2比N2效果更好,其原因是.
(2)吸收法脱硫
烟气中的SO2可以用“亚硫酸铵吸收法”处理,发生的反应为(NH4)2SO3+SO2+H2O═2NH4HSO3,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示.b点时溶液pH=7,则n():n(NH+4)=HSO-3.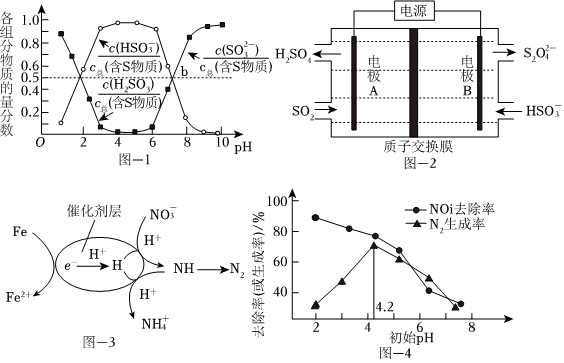
(3)电解法脱硫
用NaOH吸收后SO2,所得NaHSO3溶液经电解后可制取Na2S2O4溶液,反应装置如图-2所示。电解时每有1molS2生成有O2-4molH+透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中。其催化还原反应的过程如图-3所示。NO-3
①该反应机理中生成N2的过程可描述为.
②过程中去除率及N2生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当pH<4.2时,随pH减小,N2生成率逐渐降低的原因是NO-3。发布:2024/12/30 5:30:2组卷:43引用:4难度:0.5


