2023年北京市朝阳区高考化学二模试卷
发布:2024/5/20 8:0:9
一、选择题:本部分共14题,每题3分,共42分.在每题列出的四个选项中,选出最符合题目要求的一项.
-
1.中国“天宫”空间站使用了很多高新技术材料.下列对涉及材料的说法不正确的是( )
组卷:90引用:5难度:0.5 -
2.下列物质的应用中,与氧化还原反应无关的是( )
组卷:35引用:2难度:0.8 -
3.下列说法不正确的是( )
组卷:118引用:7难度:0.6 -
4.下列方程式与所给事实不相符的是( )
组卷:129引用:5难度:0.5 -
5.下列关于同主族元素C、Si及其化合物的性质比较和原因分析不正确的是( )
选项 性质比较 原因分析 A 熔点:CO2<SiO2 摩尔质量:CO2<SiO2 B 电负性:C>Si 原子半径:C<Si C 酸性:H2CO3>H2SiO3 非金属性:C>Si D 热稳定性:CH4>SiH4 键能:C-H>Si-H 组卷:100引用:5难度:0.8 -
6.近日科学家合成了一种新型芳香化合物K72(N6)4(N5)56(N2)72,其结构中含有
(平面正六边形,与苯的结构类似)、N4-6(平面正五边形)以及N2。下列说法不正确的是( )N-5组卷:124引用:3难度:0.5
二、非选择题
-
18.K2FeO4是一种高效多功能的新型消毒剂.
已知:K2FeO4微溶于水,在酸性或中性溶液中快速分解产生O2,在碱性溶液中较稳定.
(1)K2FeO4中铁元素的化合价为,具有强氧化性.
(2)一种制备K2FeO4的方法如图.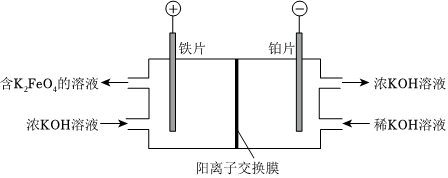
①生成K2FeO4的电极反应式:.
②阴极室KOH的浓度提高,结合电极反应式解释原因:.
(3)向含K2FeO4的溶液中加入KOH固体,析出K2FeO4固体,再用稀KOH溶液洗涤,得到K2FeO4产品.用化学方程式解释不能用水洗涤K2FeO4的原因:.
(4)称取ag制得的K2FeO4产品,加入足量NaOH、CrCl3溶液,充分反应后,加入H2SO4调节溶液pH=2,用xmol•L-1FeSO4溶液进行滴定,消耗FeSO4溶液ymL.计算K2FeO4样品的质量分数:.[已知:M(K2FeO4)=198g•mol-1]
涉及的反应有:+Cr3++3OH-=Fe(OH)3↓+FeO2-4CrO2-4
2+2H+⇌Cr2CrO2-4+H2OO2-7
Cr2+6Fe2++14H+=2Cr3++6Fe3++7H2OO2-7
(5)电解1.5h后,测得η(K2FeO4)=40%,S(K2FeO4)=60%.
已知:η(B)=×100%;S(B)=n(生成B所用的电子)(通过电极的电子)×100%.n(生成B所用的铁)n(转化的铁)
①S(K2FeO4)=60%,说明除K2FeO4之外,还有其他含铁物质生成.经检验,阳极产物中含铁物质仅有K2FeO4和FeOOH,则η(FeOOH)=.
②判断阳极有水(或OH-)放电,判断依据:
ⅰ.水(或OH-)有还原性;
ⅱ..组卷:52引用:1难度:0.5 -
19.小组同学探究Na2SO3和不同铜盐溶液的反应,实验如下.
实验:向2mL0.5mol•L-1Na2SO3溶液中加入1mL0.25mol•L-1CuCl2溶液,立即产生橙黄色沉淀(沉淀A),放置5min左右,转化为白色沉淀(沉淀B).
已知:ⅰ.Cu+Cu(NH3)2+(无色)浓氨水
ⅱ.Cu+Cu2++Cu稀硫酸
(1)研究沉淀B的成分.
向洗涤后的沉淀B中加入足量浓氨水,得到无色溶液,在空气中放置一段时间,溶液变为深蓝色.取少量深蓝色溶液,滴加试剂X,产生白色沉淀.
①白色沉淀是AgCl,试剂X是.
②无色溶液在空气中放置变为深蓝色,反应的离子方程式为.
(2)经检验,沉淀A不含。推测沉淀A能转化为沉淀B与Cl-有关,为研究沉淀A的成分及沉淀A转化为B的原因,实验如图.SO2-4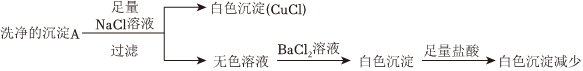
①仅通过上述实验不能证明沉淀A中含有Cl-,补充实验:向少量洗净的沉淀A中加入稀硫酸,证实沉淀A中含有Cu+的证据是.
②无色溶液中含有,推测SO2-4的产生有两个途径:SO2-4
途径1:实验过程中O2氧化;SO2-3
途径2:(将途径补充完整).
经研究,途径1不合理,途径2合理.
③解释Na2SO3和CuCl2溶液反应时,先产生橙黄色沉淀,再转化为白色的原因:.
(3)Na2SO3和CuCl2溶液反应最终生成CuCl沉淀,并检测到有SO2生成,离子方程式是.
(4)用Na2SO3和CuSO4溶液重复上述实验,仅产生橙黄色沉淀,放置72h后变为暗红色沉淀(可溶于氨水,得到无色溶液,放置变为深蓝色).
(5)根据上述实验所得结论:(答出两点).组卷:88引用:2难度:0.5


