2023年天津市耀华中学高考化学一模试卷
发布:2024/5/17 8:0:8
选择题
-
1.实现中国梦,离不开化学与科技的发展,下列有关说法错误的是( )
组卷:160引用:5难度:0.7 -
2.我国发布了《医用同位素中长期发展规划(2021-2035年)》,对提升医用同位素相关产业能力水平、保障健康中国战略实施具有重要意义。医用同位素有14C、18F、131I、60Co等,有关说法不正确的是( )
组卷:103引用:2难度:0.7 -
3.下列化学用语表示正确的是( )
组卷:108引用:1难度:0.5 -
4.下列实验操作设计正确且能达到实验目的的是( )

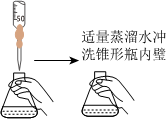
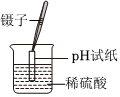
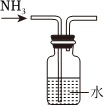
A.演示喷泉实验 B.滴定实验中用标准碱液滴定盐酸接近滴定终点的操作 C.测稀硫酸的pH D.制备氨水 组卷:223引用:5难度:0.8 -
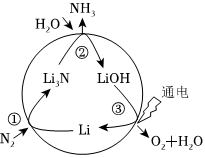 5.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是( )组卷:184引用:3难度:0.7
5.固氮是将游离态的氮转变为氮的化合物,一种新型人工固氮的原理如图所示。下列叙述正确的是( )组卷:184引用:3难度:0.7
-
15.已知甲酸铜是一种重要的化工原料,常温常压下稳定,可溶于水,难溶于乙醇,具有还原性,某实验小组在实验室用废铜屑制备甲酸铜晶体Cu(HCOO)2•4H2O,实验流程如图:

回答下列问题:
(1)若甲同学设计方案:铜屑、稀硫酸加热通入氧气制得硫酸铜溶液,再与甲酸反应生成甲酸铜溶液,再结晶。请判断:甲同学(填“能”或“不能”)制得甲酸铜晶体。
(2)步骤Ⅱ制备Cu(OH)2•CuCO3时,写出CuSO4和NaHCO3物质的量之比为1:2时的离子方程式:。
(3)操作步骤Ⅲ:向盛Cu(OH)2•CuCO3烧杯中加入一定量热蒸馏水,逐滴加入甲酸至固体恰好全部溶解,然后除去少量不溶性杂质,过程中为了防止甲酸铜结晶损失,可采取操作;接着冷却结晶,过滤,再洗涤晶体2~3次,为使固体快速干燥,可选(填写序号)来洗涤。得到产品。
A.冷水
B.乙醇
C.四氯化碳
D.饱和甲酸铜溶液
(4)晶体中甲酸根含量的测定: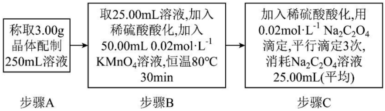
①下列仪器可供步骤A选用的是(写名称,下同);可供步骤C中滴定选用的是。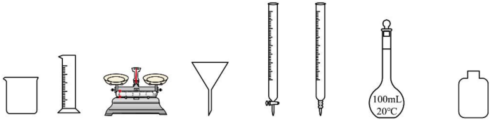
②溶液恒温80℃30min时应采取的操作方法是,步骤C滴定时当观察到即达到滴定终点。
③计算晶体中甲酸根的质量分数为。组卷:77引用:1难度:0.3 -
16.溴代烷的制备,分“氧化”和“溴化”两个过程,回答下列问题。
(1)氧化过程:HBr(g)与O2(g)在合适温度下制备Br2(g)。
已知:T℃时,相关物质的相对能量如下表所示:
此温度下,在恒容密闭容器中充入4molHBr(g)和1molO2(g),测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时,测得放出热量为QkJ,则下列关系正确的是物质 HBr(g) O2(g) H2O(g) Br2(g) 相对能量/kJ⋅mol-1 x y z w (填标号)。
A.Q=0.6(2z+2w-4x-y)
B.Q<0.6(2z+2w-4x-y)
C.Q<0.6(4x+y-2z-2w)
D.0.6(4x+y-2z-2w)<Q<4x+y-2z-2w
(2)溴化过程:在T℃下,向10V0L容器中投入初始浓度均为0.1mol⋅L-1的Br2(g)和CH4(g),发生反应:Br2(g)+CH4(g)⇌CH3Br(g)+HBr(g)。保持温度不变,压缩容器体积,分别测得不同容积下CH3Br(g)的平衡浓度如下表:
当容器体积从10V0L缩小到3V0L时,测得此时容器内仍有四种气态组分,则m=容器体积V/L 10V0 3V0 V0 c(CH3Br)/mol⋅L-1 m 0.09 0.25 ;容器体积缩小到V0L时,平衡移动(填“正向”、“逆向”或“不”)。T℃时,此反应在容积为10V0L和V0L时化学平衡常数分别为K1、K2,则K1K2(填“大于”、“小于”或“等于”)。
(3)新工艺可将甲烃、HBr和O2混合,直接催化“氧化溴化”:2CH4(g)+2HBr(g)+O2(g)⇌2CH3Br(g)+2H2O(g)ΔH<0。反应起始物料n(CH4)、n(HBr)、n(O2)分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中CH3Br的物质的量分数为x(CH3Br),在T为500℃下的x(CH3Br)~p、在p为3×105Pa下的x(CH3Br)~T如图所示: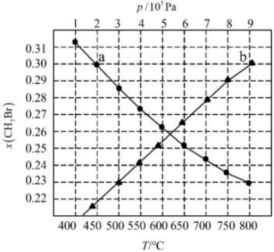
①图中a点对应的反应条件为,此时用各物质平衡分压表示的平衡常数Kp=Pa-1(列计算式,某气体分压=总压×该气体的物质的量百分数)。
②b点对应的甲烷转化率α(CH4)=(保留三位有效数字)。组卷:72引用:1难度:0.6


