当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:365
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:400
更新:2025年04月25日
|
351.为了探究铁及其化合物的氧化性和还原性,某同学设计如下实验方案,其中符合实验要求且正确的是( )
选项 实验操作 实验现象 离子反应 实验结论 A 在氯化亚铁溶液中滴加新制氯水 浅绿色溶液变成棕黄色溶液 2Fe2++Cl2═2Fe3++2Cl- Fe2+具有氧化性 B 在氯化亚铁溶液中加入锌片 浅绿色溶液变成无色溶液 Fe2++Zn═Fe+Zn2+ Zn具有还原性 C 在氯化铁溶液中加入铁粉 棕黄色溶液变成浅绿色溶液 Fe3++Fe═2Fe2+ 铁单质具有还原性 D 在氯化铁溶液中加入铜粉 棕黄色溶液变成蓝色溶液 2Fe3++Cu═2Fe2++Cu2+ Fe3+具有还原性 发布:2024/5/23 20:38:36组卷:159引用:3难度:0.8352.下列解释实验现象的反应方程式正确的是( )
发布:2024/5/23 20:38:36组卷:41引用:1难度:0.6353.以下说法错误的是( )
发布:2024/5/23 20:38:36组卷:23引用:4难度:0.9354.把Na2CO3和NaHCO3的混合物27.4 g加热到质量不再变化时,得残留固体21.2 g.求原混合物中NaHCO3和Na2CO3的质量之比为( )
发布:2024/5/23 20:38:36组卷:87引用:4难度:0.6355.实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液
用于吸收少量氧气),下列说法正确的是( )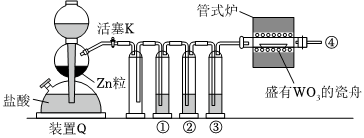 发布:2024/5/23 20:38:36组卷:41引用:4难度:0.9
发布:2024/5/23 20:38:36组卷:41引用:4难度:0.9356.A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与C同主族,可形成CA型离子化合物,D是同周期元素中简单离子半径最小的元素,B与E同主族,E2-与Ar具有相同的电子层结构,W的合金用量最大,用途最广。回答下列问题:
(1)C在元素周期表中的位置是。
(2)A分别与B、E形成的最简单化合物中沸点较高的是(填化学式),原因是。
(3)A、B、C三种元素组成的物质中含有的化学键类型是。
(4)D单质与C的最高价氧化物对应水化物的溶液反应,反应的化学方程式为。
(5)向盛有A2B2溶液的试管中加入几滴酸化的WEB4溶液,溶液变成棕黄色,发生反应的离子方程式为。发布:2024/5/23 20:38:36组卷:9引用:2难度:0.7357.用容量瓶配制一定物质的量浓度的NaCl溶液的实验中,会使所配溶液浓度偏高的是( )
发布:2024/5/23 20:38:36组卷:43引用:2难度:0.6358.下列关于氯气的说法不正确的是( )
发布:2024/5/23 20:38:36组卷:164引用:9难度:0.9359.某化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是。
(3)实验记录(在仿照①实验作答,划线部分不必填写)
(4)学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是序号 实验设计 实验观察(主要现象) 离子方程式 解释与结论 ① 在铁粉中滴
入稀硫酸铁粉溶解,溶液由无
色变成浅绿色,有无
色无味的气体生成
Fe+2H+=H2↑+Fe2+
Fe具有还原性
②氯化亚铁溶液中滴入KSCN溶液,再加入氯水 滴入KSCN溶液无明
显变化,加入氯水立
即变成血红色③ 氯化亚铁溶液加
入锌片Fe2++Zn=Fe+Zn2+
④
Fe3+具有氧化性
A、Cl2
B、Na
C、Mg2+
D、H2O2
(5)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因:;你将对实验员在配制氯化亚铁溶液时,提出的建议是。
(6)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,为帮助实验员进行检验少量Fe2+的存在,请从下列物质中选择合适的试剂
A、KSCN溶液
B、稀盐酸
C、KMnO4溶液
D、NaOH溶液。发布:2024/5/23 20:38:36组卷:47引用:6难度:0.5360.向某晶体的溶液中加入含Fe2+的溶液无明显变化,当滴加几滴溴水后,混合液出现红色,由此得出下列的结论错误的是( )
发布:2024/5/23 20:38:36组卷:55引用:14难度:0.9



