当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:1035
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1229
更新:2025年05月26日
|
31.工业上利用C和H2O(g)来制造水煤气,可以进一步制造重要的工业原料甲醇。现有4molC(s)和5molH2O(g)在一定条件下发生反应:C(s)+H2O(g)
CO(g)+H2(g)。已知反应容器容积为1L,经过10s后测得生成2molH2(g),则下列说法不正确的是( )高温发布:2024/5/23 20:38:36组卷:2引用:2难度:0.532.Na2CO3属于碱
(判断对错)发布:2024/5/23 20:38:36组卷:4引用:1难度:0.9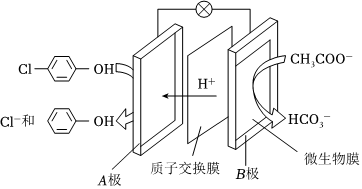 33.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
33.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(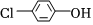 ),其原理如图所示,下列说法正确的是( )发布:2024/5/23 20:38:36组卷:31引用:4难度:0.7
),其原理如图所示,下列说法正确的是( )发布:2024/5/23 20:38:36组卷:31引用:4难度:0.734.下列物质中,其水溶液能导电,溶于水时化学键被破坏,且该物质属于非电解质的是( )
发布:2024/5/23 20:38:36组卷:12引用:6难度:0.9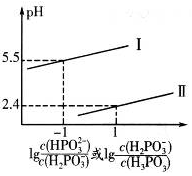 35.三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
35.三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为。
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为。
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示1g的是曲线c(HPO2-3)c(H2PO-3)(填“I”或“Ⅱ”),亚磷酸(H3PO3)的Ka1=mol•L-1,反应HPO32-+H2O⇌H2PO3-+OH-的平衡常数的值是。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6mol•L-1,则溶液中c(PO43-)=mol•L-1.(已知Ksp[Ca3(PO4)2]=2×10-29)发布:2024/5/23 20:38:36组卷:322引用:3难度:0.136.在一定温度下,CO和水蒸气分别为1mol、3mol,在密闭容器中发生反应CO+H2O(g)⇌CO2+H2,达平衡后测得CO2为0.75mol再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和可能为( )
发布:2024/5/23 20:38:36组卷:75引用:10难度:0.737.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g)△H=xkJ/mol。已知:碳的燃烧热△H1=akJ/mol。S(s)+2K(s)=K2S(s)△H2=bkJ/mol;2K(s)+N2(g)+3O2(g)=2KNO3(s)△H3=ckJ/mol,则x为( )
发布:2024/5/23 20:38:36组卷:16引用:5难度:0.838.
 南京工业大学IAM团队将蚕茧炭化形成氮掺杂的高导电炭材料,该材料作为微生物燃料电池的电极具有较好的生物相容性,提升了电子传递效率。利用该材料制备的微生物电池可降解污水中的有机物(CH3CHO为例),其装置原理如图所示。下列判断错误的是( )发布:2024/5/23 20:38:36组卷:67引用:2难度:0.5
南京工业大学IAM团队将蚕茧炭化形成氮掺杂的高导电炭材料,该材料作为微生物燃料电池的电极具有较好的生物相容性,提升了电子传递效率。利用该材料制备的微生物电池可降解污水中的有机物(CH3CHO为例),其装置原理如图所示。下列判断错误的是( )发布:2024/5/23 20:38:36组卷:67引用:2难度:0.539.下列说法不正确的是( )
发布:2024/5/23 20:38:36组卷:14引用:3难度:0.640.用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100mL 0.1000mol•L-1 NH4SCN标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 0.1000mol•L-1 AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
f.数据处理。实验序号 1 2 3 消耗NH4SCN标准溶液体积/mL 20.24 20.02 19.98
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有。
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是。
(3)滴定应在pH<0.5的条件下进行,其原因是。
(4)b和c两步操作是否可以颠倒,说明理由。
(5)所消耗的NH4SCN标准溶液平均体积为mL,测得c(I-)=mol•L-1。
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为。
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果。发布:2024/5/23 20:38:36组卷:41引用:7难度:0.6



