当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:140
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:270
更新:2025年04月25日
|
741.某温度下,在一容积固定的容器中,反应aA(g)+bB(g)⇌hH(g)达到平衡后,A.B.H的物质分别为amol、bmol、hmol,已知a+b=2h.若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是( )
发布:2024/5/23 20:38:36组卷:40引用:12难度:0.7 742.工业上以CH4为原料制备H2的原理为CH4(g)+H2O(g)═CO(g)+3H2(g)△H>0。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a、b的体积均为10L,容器a的温度为Ta容器b的温度为Tb,下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:65引用:9难度:0.5
742.工业上以CH4为原料制备H2的原理为CH4(g)+H2O(g)═CO(g)+3H2(g)△H>0。在一定条件下向a、b两个恒温恒容的密闭容器中均通入1.1mol CH4(g)和1.1mol H2O(g),测得两容器中CO的物质的量随时间的变化曲线分别为a和b。已知容器a、b的体积均为10L,容器a的温度为Ta容器b的温度为Tb,下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:65引用:9难度:0.5743.H2CO3和H2C2O4都是二元弱酸,常温下,不同pH环境下它们不同形态的粒子的组成百分率如图所示:

下列说法正确的是( )发布:2024/5/23 20:38:36组卷:80引用:5难度:0.7744.已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1。分别向1L0.5mol•L-1的NaOH溶液中加入①稀CH3COOH溶液②浓硫酸、③稀硝酸,恰好完全反应时的反应热分别为△H1、△H2、△H3,它们的关系表示正确的是( )
发布:2024/5/23 20:38:36组卷:10引用:2难度:0.5745.工业合成氨反应:N(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1,反应需要高温、高压,并且需要合适的催化剂。
(1)将1mol N2和3mol H2混合,在上述条件下使其充分反应,放出的热量总是小于92.4 kJ,其原因是。
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为mol•L-1•min-1。
(3)一定条件下,下列说法能说明合成氨的反应达到化学平衡的是。
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.反应达到最大限度
d.N2和H2的浓度相等
e.生成1molN2的同时,消耗2molNH3
f.生成3 mol H2的同时,生成2 mol NH3发布:2024/5/23 20:38:36组卷:4引用:1难度:0.6746.反应A⇌C由两步反应A→B→C构成,1molA发生反应的能量曲线如图所示。下列有关叙述正确的是( )
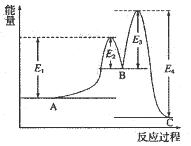 发布:2024/5/23 20:38:36组卷:8引用:3难度:0.6
发布:2024/5/23 20:38:36组卷:8引用:3难度:0.6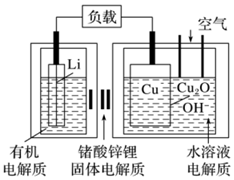 747.锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:180引用:11难度:0.7
747.锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:180引用:11难度:0.7748.能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用.某学习小组按如图所示装置探究化学能与电能的相互转化:
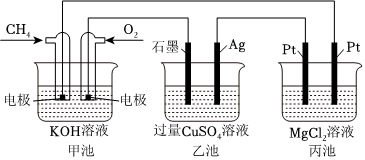
(1)甲池是装置,通入CH4气体的电极上的反应式为.乙池中移向SO2-4电极(填“石墨”或“Ag”)
(2)当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化mol,乙池若要恢复电解前的状态则需要加入g(填物质名称).
(3)丙池中发生的电解反应的离子方程式为.发布:2024/5/23 20:38:36组卷:30引用:6难度:0.3749.当用酸滴定碱时,下列操作中会使测定结果(碱的浓度)偏低的是( )
发布:2024/5/23 20:38:36组卷:61引用:8难度:0.7750.常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A.根据题意回答下列问题:
(1)写出酸H2A的电离方程式。
(2)若溶液M由10mL 2mol•L-1NaHA溶液与10mL 2mol•L-1NaOH溶液混合而得,则溶液M的pH7 (填“>”、“<”或“=”),溶液中离子浓度由大到小顺序为。(溶液混合时体积变化忽略)。
(3)已知难溶电解质MmAn在水溶液中存在溶解平衡,该难溶电解质的溶解平衡表达式为,其溶度积表达式为。已知某温度下难溶电解质硫酸银在水溶液中Ksp=1.08×10-16,把1克硫酸银投入20毫升水中,充分溶解后,溶液中C(Ag+)=。
(4)25℃时,a mol/L 氨水和0.01mol/L盐酸等体积混合充分反应后,C()═C(Cl-),求氨水的电离常数K=NH+4。发布:2024/5/23 20:38:36组卷:241引用:2难度:0.5



