当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:126
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:269
更新:2025年04月25日
|
751.肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图。已知200℃时:反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g)△H1=-32.9 kJ•mol-1;反应Ⅱ:N2H4(g)+H2(g)=2NH3(g)△H2=-41.8 kJ•mol-1
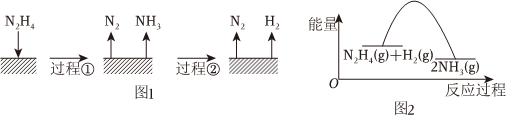
下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:28引用:5难度:0.6752.工业上为了处理含有Cr2O
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量已低于排放标准.关于上述方法,下列说法错误的是( )2-7发布:2024/5/23 20:38:36组卷:8引用:7难度:0.7753.如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色.下列说法正确的是( )
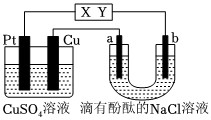 发布:2024/5/23 20:38:36组卷:64引用:16难度:0.5
发布:2024/5/23 20:38:36组卷:64引用:16难度:0.5754.(1)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol•L-1酸性KMnO4溶液和未知浓度的无色NaHSO3溶液。反应的离子方程式是2MnO4-+5HSO3-+H+═2Mn2++5SO42-+3H2O。
请完成下列各题:
①该滴定实验所需仪器有下列中的。
A.酸式滴定管(50mL)
B.碱式滴定管(50mL)
C.量筒(10mL)
D.锥形瓶
E.铁架台
F.滴定管夹
G.烧杯
H.白纸
I.胶头滴管
J.漏斗
②本实验(填“需要”或“不需要”)使用指示剂,理由是。
(2)一定物质的量浓度溶液的配制和酸碱中和滴定是中学化学中两个典型的定量实验,某研究性学习小组在实验室中配制1mol•L-1稀硫酸标准溶液。然后用其滴定某未知浓度的NaOH溶液。下列有关说法中正确的是。
A.实验中所用到的滴定管、容量瓶在使用前均需要查漏
B.若选用100mL容量瓶配制标准酸溶液,需用密度为1.84g•mL-1、98%的浓硫酸5.43mL
C.容量瓶中有少量的蒸馏水,会导致所配标准溶液的浓度偏小
D.酸式滴定管用蒸馏水洗涤后,即装入标准浓度的稀硫酸,则测得的NaOH溶液的浓度将偏大
E.若配制标准酸溶液在定容时俯视刻度线,则导致所测的NaOH溶液浓度偏大
F.中和滴定实验,若滴定前平视读数、滴定结束俯视读数,则导致实验结果偏大发布:2024/5/23 20:38:36组卷:20引用:1难度:0.6755.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产ZnSO4•6H2O晶体,其工艺流程如图,有关氢氧化物沉淀时的pH如下表。

(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有氢氧化物 Al(OH)3 Fe(OH)3 Fe(OH)2 Zn(OH)2 开始沉淀的pH 3.3 1.5 6.5 5.4 沉淀完全的pH 5.0 3.7 9.7 8.0 。
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是;为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液pH范围是;为控制上述pH范围可选择加入的试剂或药品是。
A.ZnO
B.氨水
C.固体NaOH
D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是。“操作A”的名称是。
(4)常温下,已知Ksp[Cu(OH)2]=2.0×10-20,某CuSO4溶液里c(Cu2+)=2.0×10-4mol/L,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于。发布:2024/5/23 20:38:36组卷:248引用:2难度:0.5756.已知反应:
①CO(g)+CuO(s)⇌CO2(g)+Cu(s) K1
②H2(g)+CuO(s)⇌Cu(s)+H2O(g) K2
③CO(g)+H2O(g)⇌CO2(g)+H2(g) K
T1时的平衡常数分别为K1、K2和K。则下列说法正确的是( )发布:2024/5/23 20:38:36组卷:9引用:1难度:0.7757.“钙基固硫”是将煤中的硫元素以CaSO4的形式固定脱去,但煤炭燃烧过程中产生的CO又会发生如下反应,导致脱硫效率降低。
反应Ⅰ:CaSO4(s)+CO(g)═CaO(s)+SO2(g)+CO2(g)ΔH1=+218.4kJ•mol-1
反应Ⅱ:CaSO4(s)+4CO(g)═CaS(s)+4CO2(g)ΔH2=-175.6kJ•mol-1某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程中能量变化示意图正确的是( )发布:2024/5/23 20:38:36组卷:11引用:4难度:0.6758.H2C2O4为二元弱酸,Ka1(H2C2O4)=5.4×10-2,Ka2(H2C2O4)=5.4×10-5,设H2C2O4溶液中c(总)=c(H2C2O4)+c(HC2
)+c(C2O-4)。室温下用NaOH溶液滴定25.00mL 0.1000 mol•L-1 H2C2O4溶液至终点。滴定过程得到的下列溶液中微粒的物质的量浓度关系一定正确的是( )O2-4发布:2024/5/23 20:38:36组卷:8引用:3难度:0.5759.下列说法不正确的是( )
发布:2024/5/23 20:38:36组卷:9引用:2难度:0.8760.某温度下,密闭容器中发生反应aX(g)⇌bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍.则下列叙述正确的是( )
发布:2024/5/23 20:38:36组卷:104引用:48难度:0.7



