当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:391
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:410
更新:2025年04月25日
|
291.“碘伏”又叫“聚维酮碘溶液”。聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如下:
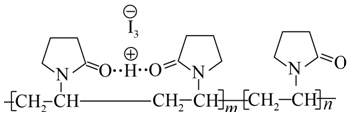
(图中虚线表示氢键)。下列说法正确的( )发布:2024/5/23 20:38:36组卷:83引用:5难度:0.7292.下列说法正确的是( )
发布:2024/5/23 20:38:36组卷:45引用:4难度:0.6293.下列说法中正确的是( )
发布:2024/5/23 20:38:36组卷:63引用:5难度:0.5294.(1)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间结构是;N2H4分子中氮原子轨道的杂化类型是。
②肼可用作火箭燃料,燃烧时发生的反应:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)ΔH=-1038.7kJ•mol-1若该反应中有4molN-H键断裂,则形成的π键有mol。
(2)H2Se的酸性比H2S(填“强”或“弱”)。气态SeO3分子的空间结构为,SO32-的空间结构为。发布:2024/5/23 20:38:36组卷:8引用:1难度:0.6295.下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定.发布:2024/5/23 20:38:36组卷:76引用:4难度:0.5296.碳和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。粗硅的制备有二种方法:
方法一:SiO2+2CSi+2CO↑ 方法二:SiO2+2Mg高温Si+2MgO高温
(1)基态硅原子中存在对自旋相反的电子,基态Mg 的最外层电子所占据的能级的电子云能廓图是。
(2)上述反应中所有元素第一电离能最小的元素是(填元素符号)。
(3)试比较C (金刚石),晶体Si,CO 三种物质的熔沸点从高到低的顺序,试解释原因:。
(4)CO 在配合物中可作为配体,在Cr(CO)6配合物中配原子是(填元素符号)1mol该配合物中含有π键的数目。
(5)SiO2晶跑(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si-Si之间插入O原子而形成。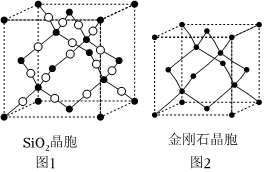
①推测SiO2晶胞中Si采用杂化,O-Si-O的键角。
②SiO2晶跑中,含有Si原子个和O原子个。
③假设金刚石晶胞的边长为apm,试计算该晶胞的密度g/cm3 (写出表达式即可)。发布:2024/5/23 20:38:36组卷:20引用:5难度:0.4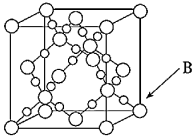 297.我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大.元素A、B、C、D、E的原子结构等信息如下:
297.我国从国外进口某原料经测定主要含有A、B、C、D、E五种前四周期元素,且原子序数依次增大.元素A、B、C、D、E的原子结构等信息如下:
请回答下列问题:(用A、B、C、D、E,所对应的元素符号作答)元素 元素性质或原子结构 A 周期表中原子半径最小的元素 B 原子核外有三种不同的能级且各个能级所填充的电子数相同 C 最外层P轨道半充满 D 位于短周期,其原子的核外成对电子数是未成对电子数的3倍 E 位于ds区且原子的最外层电子数与A的相同
(1)B、C、D第一电离能由大到小为.
(2)E的二价离子的电子排布式为.
(3)A2B2D4常用作除锈剂,该分子中B的杂化方式为;1molA2B2D4分子中含有σ键数目为.
(4)与化合物BD互为等电子体的阴离子化学式为;
(5)B2A6、C2A4分子中均含有18个电子,它们的沸点相差较大,主要原因是.
(6)BD2在高温高压下所形成晶体的晶胞如图所示,一个该晶胞中含个D原子.发布:2024/5/23 20:38:36组卷:46引用:6难度:0.3298.下列叙述正确的是( )
发布:2024/5/23 20:38:36组卷:13引用:5难度:0.7299.元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是.
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是.
(3)Y 与Z 可形成YZ42-
①YZ42-的空间构型为(用文字描述).
②写出一种由第三周期元素组成的与YZ42-互为等电子体的分子的化学式:.
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为.发布:2024/5/23 20:38:36组卷:12引用:2难度:0.5300.下图是从NaCl或CsCl晶体结构图中分割出来的部分结构图,其中属于从NaCl晶体中分割出来的结构图是( )
 发布:2024/5/23 20:38:36组卷:169引用:18难度:0.7
发布:2024/5/23 20:38:36组卷:169引用:18难度:0.7



