当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
热点预测
中考复习
热搜题专练
浏览次数:459
更新:2025年04月27日
|
 已完结
已完结
|
热点预测
高考复习
新题抢练
浏览次数:447
更新:2025年04月25日
|
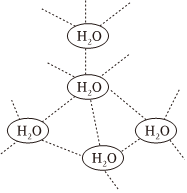 391.水分子间可通过“氢键”彼此结合而形成(H2O)n,在冰中n值为5,即每个水分子都被其他4个水分子包围形成变形四面体,由无限个这样的四面体通过氢键相互连接成一个庞大的分子晶体,即冰--如图所示的(H2O)5单元结构。下列有关叙述正确的是( )发布:2024/5/23 20:38:36组卷:41引用:4难度:0.6
391.水分子间可通过“氢键”彼此结合而形成(H2O)n,在冰中n值为5,即每个水分子都被其他4个水分子包围形成变形四面体,由无限个这样的四面体通过氢键相互连接成一个庞大的分子晶体,即冰--如图所示的(H2O)5单元结构。下列有关叙述正确的是( )发布:2024/5/23 20:38:36组卷:41引用:4难度:0.6392.在HF、H2O、NH3、CS2、CH4、N2、BF3分子中:
(1)以非极性键结合的非极性分子是。
(2)以极性键结合的具有直线形结构的非极性分子是。
(3)以极性键结合的具有正四面体形结构的非极性分子是。
(4)以极性键结合的具有三角锥形结构的极性分子是。
(5)以极性键结合的具有sp3杂化轨道结构的分子是。
(6)以极性键结合的具有sp2杂化轨道结构的分子是。发布:2024/5/23 20:38:36组卷:59引用:3难度:0.6393.我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2
CO2+H2O.下列有关说法正确的是( )催化剂发布:2024/5/23 20:38:36组卷:56引用:5难度:0.5394.纳米TiO2是一种重要的光催化剂,以钛酸四丁酯为原料制备它的原理是:Ti(OC4H9)4+2H2O
4C4H9OH+TiO2。回答下列问题:一定条件
(1)钛在周期表中位于区。下列状态对应的氧粒子中,失去一个电子所需要能量最小的是
(填字母)。
A.1s22s22p4
B.1s22s22p3
C.1s22s22p33s1
D.1s22s22p2
(2)C4H9OH中(填“是”或“否”)存在正四面体结构。H2O分子的空间构型为。Ti(OC4H9)4中存在配位键,其中提供孤电子对的原子是。
(3)C4H9OH中碳原子、氧原子的杂化类型分别为;已知正丁醇的熔点、沸点分别为-89℃、117.7℃,1-氯丁烷的熔点、沸点分别为-123.1℃、78℃,存在这种差异的主要原因是。
(4)二氧化钛的一种晶胞结构如图所示,则钛原子的配位数为,若氧原子、钛原子的半径分别为rOpm、rTipm,晶胞体积为Vcm3,则该晶胞中原子的空间利用率是(用含rO、rTi、V、π的式子表示)。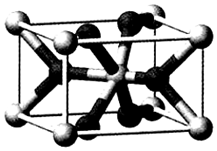 发布:2024/5/23 20:38:36组卷:7引用:1难度:0.4
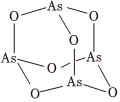
发布:2024/5/23 20:38:36组卷:7引用:1难度:0.4395.As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AsH3下列说法正确的是( )
 发布:2024/5/23 20:38:36组卷:72引用:4难度:0.7
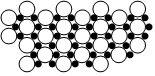
发布:2024/5/23 20:38:36组卷:72引用:4难度:0.7396.2001年3月发现硼化镁在39K时呈超导性,可 能是人类对超导认识的新里程碑.在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼的相间排列,如图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上.根据下图确定硼化镁的化学式为( )
 发布:2024/5/23 20:38:36组卷:65引用:5难度:0.9
发布:2024/5/23 20:38:36组卷:65引用:5难度:0.9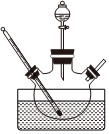 397.实验室通常是在NH3和NH4Cl存在条件下,以活性炭为催化剂,用H2O2氧化CoCl2溶液来制备三氯化六氨合钴[Co(NH3)6]Cl3,该反应属于大量放热的反应。某小组用如图所示装置制备[Co(NH3)6]Cl3,实验步骤如下:
397.实验室通常是在NH3和NH4Cl存在条件下,以活性炭为催化剂,用H2O2氧化CoCl2溶液来制备三氯化六氨合钴[Co(NH3)6]Cl3,该反应属于大量放热的反应。某小组用如图所示装置制备[Co(NH3)6]Cl3,实验步骤如下:
Ⅰ.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,逐滴加入5mL 30%的H2O2溶液。
Ⅱ.用水浴将混合物加热至60℃,恒温20分钟,然后用冰水浴冷却,充分结晶后过滤。
Ⅲ.将沉淀溶于热的盐酸中,趁热过滤,滤液中加适量浓盐酸并冷却结晶。
Ⅳ.过滤、用乙醇洗涤晶体并在105℃条件下烘干。
试回答下列问题:
(1)制备[Co(NH3)6]Cl3的化学方程式是。
(2)请指出装置中存在的一处缺陷。
(3)若将5mL 30%的H2O2溶液一次性加入三颈烧瓶,会出现的问题是。
(4)与[Co(NH3)6]Cl3类似的产品还有[Co(NH3)5Cl]Cl2,请简述验证某晶体是[Co(NH3)6]Cl3还是[Co(NH3)5•Cl]Cl2的实验方案。
(5)步骤Ⅲ中趁热过滤的主要目的是,滤液中加适量浓盐酸的主要目的是。
(6)乙醇洗涤与蒸馏水洗涤相比优点是。发布:2024/5/23 20:38:36组卷:43引用:4难度:0.5398.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D形成的二价阳离子与C形成的简单阴离子具有相同的电子层结构。AC2为非极性分子。B、C的简单氢化物的沸点比它们同主族相邻周期元素的氢化物的沸点高。E是前四周期中原子核外电子排布中未成对电子数最多的元素。请根据以上情况,回答下列问题:
(1)A、B、C的电负性由小到大的顺序为(用对应元素符号表示,下同)
(2)A的氢化物中有一种组成为A2H2的分子,其中A原子的轨道杂化类型为,1molA2H2所含σ键的数目为。
(3)写出化合物AC2的电子式:。
(4)E的价电子排布式是。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是。发布:2024/5/23 20:38:36组卷:32引用:2难度:0.5399.(1)在碱金属元素中,锂的金属性最弱,其原因是
。锂在氧气中燃烧所得产物的化学键类型是。
(2)在周期表中,锂的性质与镁相似,预测锂在氮气中燃烧的化学方程式:。碳酸锂、硫酸锂的溶解性依次为、。(填“易溶”、“微溶”或“难溶”)
(3)锂在自然界中存在的主要形式为锂辉石(LiAlSi2O6)、锂云母[Li2F2Al2(SiO3)3]等。锂辉石(LiAlSi2O6)中化合价最高的元素和锂云母[Li2F2Al2(SiO3)3]中非金属性最强的元素组成的化合物的电子式,它是(填“离子化合物”或“共价化合物”)。常温常压下,它呈态,原因是。
(4)四氢硼锂(LiBH4)、四氢铝锂(LiAlH4)都是重要还原剂,在有机合成中用途广泛。比较半径:r(Li+)r(H-)(填“>”、“<”或“=”),理由是。发布:2024/5/23 20:38:36组卷:31引用:1难度:0.6400.第四周期过渡金属元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)镍铬钢抗腐蚀性能强,Ni2+基态原子的核外电子排布为,铬元素在周期表中区。
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN═Fe(SCN)3+3KCl表示。经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显红色。含该离子的配合物的化学式是。
②铁的另一种配合物铁氰化钾K3[Fe(CN)6]俗称赤血盐,可用于检验Fe2+,两者反应生成带有特征蓝色的沉淀,该赤血盐中心原子的配位数,请写出一种与其配体互为等电子体的分子:。发布:2024/5/23 20:38:36组卷:37引用:2难度:0.6



