当前位置:
章节挑题
请展开查看知识点列表
>
更多>>
 已完结
已完结
|
期末复习
典型试卷
考前必刷
浏览次数:1131
更新:2025年06月03日
|
 已完结
已完结
|
热点预测
高考复习
难题抢练
浏览次数:1249
更新:2025年05月26日
|
71.下列物质用途或操作正确且与盐类水解有关的一组是( )
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用TiCl4水溶液制备TiO2•xH2O
③用氯化铁溶液和氨水制备氢氧化铁胶体
④除去氯化铜溶液中的氯化铁杂质,可在溶液中加入过量的氧化铜,过滤除杂
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制Fe(NO3)2溶液时将Fe(NO3)2晶体溶于浓硝酸中并加入蒸馏水稀释至指定浓度
⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火发布:2024/5/23 20:38:36组卷:138引用:7难度:0.7 72.某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )发布:2024/5/23 20:38:36组卷:230引用:6难度:0.5
72.某温度下,将pH和体积均相同的HCl和CH3COOH溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )发布:2024/5/23 20:38:36组卷:230引用:6难度:0.5 73.可逆反应A(?)+aB(g)⇌C(g)+D(g).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:175引用:6难度:0.7
73.可逆反应A(?)+aB(g)⇌C(g)+D(g).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )发布:2024/5/23 20:38:36组卷:175引用:6难度:0.774.某同学利用Cl2氧化K2MnO4制备KMnO4的装置如图所示(夹持装置略):

已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3+2H2O═2MnO2-4+MnO2↓+4OH-MnO-4
回答下列问题:
(1)装置A中a的作用是;装置C中的试剂为;装置A中制备Cl2的化学方程式为。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入(填“酸式”或“碱式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO4溶液起始读数为15.00mL,此时滴定管中KMnO4溶液的实际体积为(填标号)。
A.15.00mL
B.35.00mL
C.大于35.00mL
D.小于15.00mL
(4)某FeC2O4•2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4•2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.称取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃.用c mol•L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。
样品中所含H2C2O4•2H2O(M=126g•mol-1)的质量分数表达式为。
下列关于样品组成分析的说法,正确的是(填标号)。
A.=3时,样品中一定不含杂质V1V2
B.越大,样品中H2C2O4•2H2O含量一定越高V1V2
C.若步骤Ⅰ中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D.若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高发布:2024/5/23 20:38:36组卷:814引用:12难度:0.375.一定条件下A、B、C的如图所示的转化关系,且△H=△H1+△H2.则A、C可能是( )

①Fe、FeCl3
②C、CO2
③AlCl3、NaAlO2
④NaOH、NaHCO3
⑤S、SO3
⑥Na2CO3、CO2。发布:2024/5/23 20:38:36组卷:226引用:10难度:0.776.(1)如图表示使用新型电极材料,以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式:
。生产中可分离出的物质A的化学式为。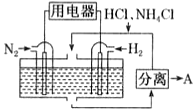
(2)电化学降解治理水中硝酸盐污染。在酸性条件下,电化学降解NO3-的原理如图所示,阴极反应式为。假设降解前两极溶液质量相等,当电路中有2mol电子通过时,此时两极溶液质量的差值为g。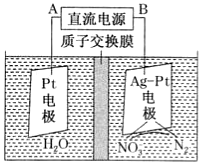
(3)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3 的ZrO2固体,它在高温下能传导正极生成的O2-。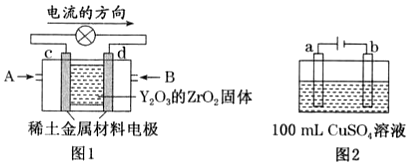
①d电极的名称为该电极的电极反应式为。
②如图2所示为用惰性电极电解100mL0.5mol•L-1CuSO4溶液,a电极上的电极反应式为。发布:2024/5/23 20:38:36组卷:4引用:2难度:0.6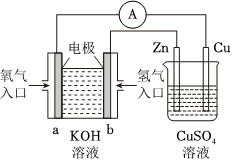 77.关于如图所示装置的判断,叙述正确的是( )发布:2024/5/23 20:38:36组卷:25引用:3难度:0.7
77.关于如图所示装置的判断,叙述正确的是( )发布:2024/5/23 20:38:36组卷:25引用:3难度:0.778.下列依据实验操作及现象得出的结论正确的是( )
选项 实验操作 现象 结论 A 向CuSO4溶液中通入H2S 生成黑色沉淀(CuS) H2S的酸性比H2SO4强 B 向等体积等浓度的盐酸中分别加入ZnS和 CuS ZnS溶解而CuS不溶解 Ksp(CuS)<Ksp(ZnS) C 向NaCl和NaBr混合溶液中滴加少量AgNO3溶液 出现淡黄色沉淀(AgBr) Ksp(AgCl)<Ksp(AgBr) D 常温下,用pH计分别测0.1mol/LNaA溶液、0.1mol/L Na2CO3溶液的pH NaA溶液的pH小于Na2CO3溶液的pH 酸性:HA>H2CO3 发布:2024/5/23 20:38:36组卷:1引用:1难度:0.579.如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
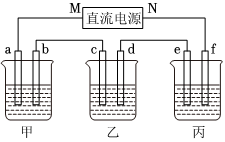
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
①电源的N端为极;
②电极b上发生的电极反应为;
③电极b上生成的气体在标准状况下的体积:;
④电极c的质量变化是g;
⑤电解前后各溶液的pH值的变化(填“不变”、“变大”或“变小”)
甲溶液,乙溶液,丙溶液;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?.发布:2024/5/23 20:38:36组卷:39引用:11难度:0.580.在一定条件下,CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)═2CO2(g)△H=-566kJ•mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1
由1mol CO(g)和3mol CH4(g)组成的混合气体在上述条件下充分燃烧,恢复至室温释放的热量为( )发布:2024/5/23 20:38:36组卷:66引用:34难度:0.9



