某硫酸钠粗品含有少量CaCl2和MgCl2,实验室进行提纯的流程如下:
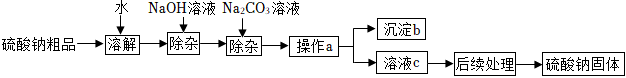
(1)加入NaOH溶液的目的是 除去MgCl2除去MgCl2。
(2)用Na2CO3溶液除杂时,发生反应的化学方程式为 Na2CO3+CaCl2=CaCO3↓+2NaClNa2CO3+CaCl2=CaCO3↓+2NaCl。
(3)操作a的名称是 过滤过滤,若NaOH和Na2CO3溶液添加过量,可在操作a 后后(填“前”或“后”)加入适量的 稀硫酸或稀H2SO4稀硫酸或稀H2SO4(填名称)除去。
(4)若“后续处理”的操作是蒸发,在进行该操作时,当蒸发皿中 出现较多固体时出现较多固体时即可停止加热。蒸发时用玻璃棒搅拌,目的是 防止因局部温度过高,造成液滴飞溅防止因局部温度过高,造成液滴飞溅。若加入的NaOH和Na2CO3溶液为适量,上述流程仍存在一处明显缺陷,请指出:没有除去反应生成的NaCl没有除去反应生成的NaCl。
(5)最终得到的硫酸钠质量 >>(填“>”或“<”或“=”)硫酸钠粗品中所含的硫酸钠质量。
【答案】除去MgCl2;Na2CO3+CaCl2=CaCO3↓+2NaCl;过滤;后;稀硫酸或稀H2SO4;出现较多固体时;防止因局部温度过高,造成液滴飞溅;没有除去反应生成的NaCl;>
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/28 8:0:9组卷:10引用:2难度:0.5
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
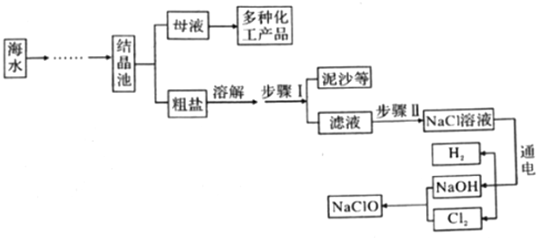
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
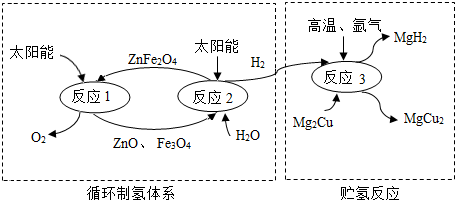 2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5 -
3.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7


