1943年我国化学家侯德榜创立了著名的“侯氏制碱法”,即将索尔维制碱法和合成氨法两种工艺联合起来,促进了世界制碱技术的发展,其工业流程如图所示。
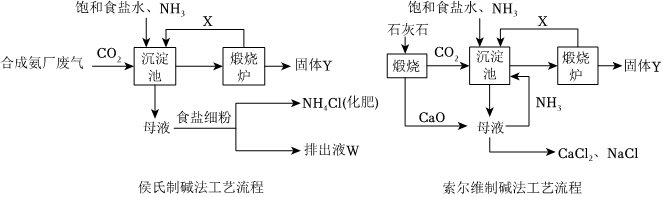
(1)侯氏制碱法中X的化学式为 CO2CO2,除X可以循环使用外,图中物质中 NaClNaCl也可循环使用。
(2)根据下表相关数据分析,沉淀池中最后析出的是NaHCO3,从离子反应和物质的量浓度的角度解释原因 钠离子和碳酸氢根离子生成溶解度较小的碳酸氢钠,碳酸氢钠首先达到饱和结晶析出,导致溶液中碳酸氢根离子、钠离子向生成碳酸氢钠的方向移动,使得在沉淀池中最后析出的是NaHCO3钠离子和碳酸氢根离子生成溶解度较小的碳酸氢钠,碳酸氢钠首先达到饱和结晶析出,导致溶液中碳酸氢根离子、钠离子向生成碳酸氢钠的方向移动,使得在沉淀池中最后析出的是NaHCO3。
相关物质的溶解度数据以及对应的饱和溶液的物质的量浓度(20℃)
| 相关物质 | NaCl | NH4Cl | Na2CO3 | NaHCO3 | NH4HCO3 |
| 对应浓度(mol/L) | ≈5 | ≈5.5 | ≈1.52 | ≈1 | ≈2.4 |
原料易获得、NaCl的利用率高、产生的氯化铵可以当作肥料
原料易获得、NaCl的利用率高、产生的氯化铵可以当作肥料
(写出一条即可)。(4)工业纯碱中可能混有少量NaCl,同学们对工业纯碱样品展开探究。
| 实验操作 | 现象 | 结论 |
| 取样品加水溶解,加入过量稀盐酸至反应完全 | 有气泡产生 | 样品中有NaCl |
| 向上述溶液中继续滴加适量AgNO3溶液 | 有 白色沉淀 白色沉淀 产生 |
B
B
(填字母)代替稀盐酸。A.CaCl2溶液
B.稀硝酸
C.BaCl2溶液
D.稀硫酸
(5)测定纯碱样品中Na2CO3的质量分数(假设杂质只有NaHCO3,并且杂质分布均匀)。称取6.14g样品溶于水,配成100mL溶液。取出25.00mL该溶液,然后向溶液中滴加0.5mol/LBa(OH)2溶液至30.00mL时恰好完全沉淀。
①加入的Ba(OH)2溶液中溶质的物质的量为
0.015
0.015
mol。②样品中n(Na2CO3):n(NaHCO3)=
5:1
5:1
。【考点】纯碱工业(侯氏制碱法).
【答案】CO2;NaCl;钠离子和碳酸氢根离子生成溶解度较小的碳酸氢钠,碳酸氢钠首先达到饱和结晶析出,导致溶液中碳酸氢根离子、钠离子向生成碳酸氢钠的方向移动,使得在沉淀池中最后析出的是NaHCO3;原料易获得、NaCl的利用率高、产生的氯化铵可以当作肥料;白色沉淀;B;0.015;5:1
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/6 5:0:8组卷:167引用:2难度:0.7
相似题
-
1.以NaCl为原料,可制取纯碱。Na2CO3可用侯氏制碱法制取,主要涉及如下反应:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3
Na2CO3+CO2↑+H2O,下列有关实验室模拟侯氏制碱法的实验原理和装置正确的是( )△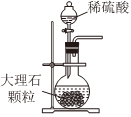
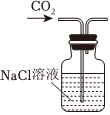
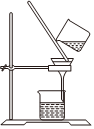
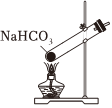
A.制取CO2 B.制取NaHCO3 C.分离NaHCO3 D.制取Na2CO3 发布:2024/12/8 18:0:1组卷:170引用:5难度:0.8 -
2.“侯氏制碱法”的主要过程如图(部分物质已略去)。
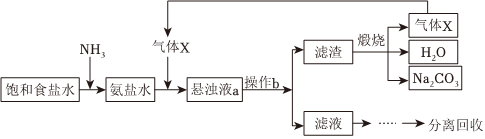
下列说法错误的是( )发布:2024/12/8 0:0:1组卷:135引用:4难度:0.7 -
3.氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,下列表达正确的是( )
氨碱法 联合制碱法 A 原料 食盐、氨气、生石灰 食盐、氨气、二氧化碳 B 副产物 氯化钙 氯化铵 C 循环物质 氨气、二氧化碳 氯化钠 D 评价 原料易得、设备简单、能耗低 原料利用率高、废弃物少 发布:2024/12/16 6:0:1组卷:38引用:2难度:0.8


