汽车工业的发展得益于化工等行业的支撑。
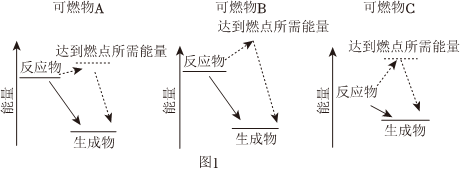
(1)三种可燃物在空气中发生燃烧反应的能量变化示意图如图,你认为可燃物 BB(填“A”、“B”或“C”)更适合用作车用燃料。(已知:燃点是指在规定的条件下,应用外部热源使物质表面起火并持续燃烧一定时间所需的最低温度,燃点较低时存在安全隐患)
(2)燃油汽车尾气有污染,尾气中NO生成过程中的能量变化如图所示。
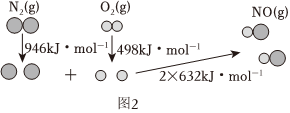
生成1mol NO(g) 吸收吸收(填“吸收”或“放出”) 9090kJ的热量。
(3)利用催化技术可将汽车尾气中的CO和NO转化为CO2和N2,化学方程式为:2NO+2CO催化剂△2CO2+N2
①某温度下,在容积2L的密闭容器中通入CO和NO,测得不同时间n(CO)如下表:
催化剂
△
| 时间/s | 0 | 1 | 2 | 3 | •••••• |
| n(CO)/mol | 7.20×10-3 | 6.10×10-3 | 5.70×10-3 | 5.50×10-3 | •••••• |
1.875×10-4mol•L-1s-1
1.875×10-4mol•L-1s-1
。②下列可以表明上述反应已达到平衡状态的是
acd
acd
。a.容器中的气体压强保持不变
b.NO、CO、CO2、N2的浓度之比为2:2:2:1
c.N2的浓度不再改变
d.相同时间内,反应消耗2mol NO同时消耗1mol N2
(4)国家电投氢能公司全自主研发的“氢腾”燃料电池系统广泛应用于氢能大巴。某种氢燃料电池的内部结构如图,下列说法正确的是
A
A
。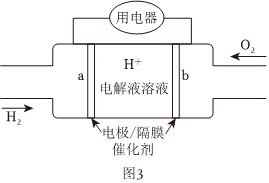
A.电池工作时,电解质溶液中的H+向b极移动
B.a极发生的电极反应为H2+2e-+2OH-═2H2O
C.b极为正极,发生氧化反应
D.当外电路有1mol电子转移时,b极消耗5.6LO2
【答案】B;吸收;90;1.875×10-4mol•L-1s-1;acd;A
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/12 8:0:9组卷:22引用:1难度:0.6
相似题
-
1.在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)⇌C(g)+D(g)已达到平衡状态( )
①混合气体的压强
②混合气体的密度
③B的物质的量浓度
④混合气体的总物质的量
⑤混合气体的平均相对分子质量
⑥v(C)与v(D)的比值
⑦混合气体的总质量.发布:2024/12/30 19:30:2组卷:40引用:3难度:0.7 -
2.二甲醚(DME)一种清洁的替代燃料,不含硫,不会形成微粒,而且与汽油相比,排放的NO2更少,因此是优良的柴油机替代燃料。工业上利用一步法合成二甲醚的反应如下(复合催化剂为CuO/ZnO/Al2O2):
2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)△H=-204.7kJ/mol
(1)若反应在恒温、恒压下进行,以下叙述能说明该反应达到平衡状态的是
A.CO和H2的物质的量浓度比是1:2
B.CO的消耗速率等于CH3OCH3的生成速率的2倍
C.容器中混合气体的体积保持不变
D.容器中混合气体的平均摩尔质量保持不变
E.容器中混合气体的密度保持不变
(2)600℃时,一步法合成二甲醚过程如下:
CO(g)+2H2(g)═CH3OH(g)△H1=-100.46kJ/mol
2CH3OH(g)═CH3OCH3(g)+H2O(g)△H2
CO(g)+H2O(g)═CO2(g)+H2(g)△H3=-38.7kJ/mol
则△H2=。
(3)复合催化剂的制备方法之一是Na2CO3共沉淀法:制备1mol/L的硝酸铜,硝酸锌和硝酸铝的水溶液。然后向盛有去离子水的烧杯中同时滴加混合硝酸盐溶液和1mol/L的Na2CO3水溶液,70℃下搅拌混合。沉淀后过滤,洗涤沉淀物,80℃下干燥12小时,然后500℃下焙烧16小时。
请写出上述过程中硝酸铝与Na2 CO3水溶液反应的离子方程式:
(4)以DME为燃料,氧气为氧化剂,在酸性电解质溶液中用惰性电极制成燃料电池,则通入氧气的电极是电源的(填正、负)极,通DME的电极反应为。发布:2025/1/3 8:0:1组卷:18引用:1难度:0.5 -
3.在一定温度下的定容容器中,反应:A(s)+2B(g)⇌C(g)+D(g)。下列不能表明反应达到平衡状态的是( )
发布:2024/12/30 19:0:1组卷:110引用:4难度:0.8


