(一)现有以下物质:①碳棒②盐酸③H2SO4④氨水⑤熔融KOH ⑥NH3⑦CCl4 ⑧CO2 ⑨CH3COOH ⑩NaHSO4固体
(1)上述物质中,属于非电解质的是 ⑥⑦⑧⑥⑦⑧。
(2)上述物质中,属于电解质的是 ③⑤⑨⑩③⑤⑨⑩。
(3)写出③、⑩两种物质在水溶液中的电离方程式。③:H2SO4=2H++SO2-4H2SO4=2H++SO2-4;⑩:NaHSO4=Na++H++SO2-4NaHSO4=Na++H++SO2-4。
(二)向Na2CO3和NaHCO3的混合溶液中逐滴加入0.2mol•L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。
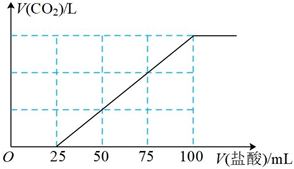
(4)则加入盐酸的体积25mL之前发生反应的离子方程式为 CO2-3+H+=HCO-3CO2-3+H+=HCO-3,产生CO2在标准状况下的体积为 336336mL,混合溶液溶质的物质的量之比为n(Na2CO3):n(NaHCO3)=1:21:2。
SO
2
-
4
SO
2
-
4
SO
2
-
4
SO
2
-
4
CO
2
-
3
HCO
-
3
CO
2
-
3
HCO
-
3
【答案】⑥⑦⑧;③⑤⑨⑩;H2SO4=2H++;NaHSO4=Na++H++;+H+=;336;1:2
SO
2
-
4
SO
2
-
4
CO
2
-
3
HCO
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/27 10:35:59组卷:60引用:1难度:0.5


