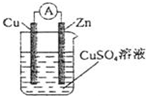
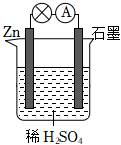
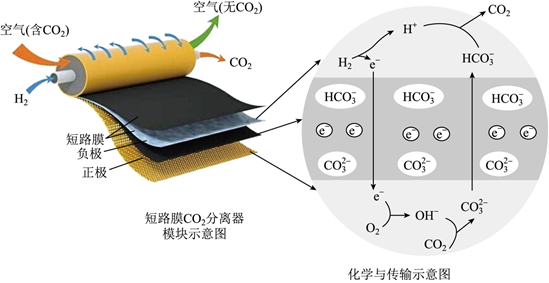
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答下列问题:
(1)A极是电源的 正极正极,一段时间后,甲中溶液颜色 颜色变浅颜色变浅,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 氢氧化铁胶体粒子带正电荷氢氧化铁胶体粒子带正电荷,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、E电极均只有一种单质生成时,对应单质的物质的量之比为 1:21:2。
(3)现用丙装置给铜件镀银,则G应是 镀层金属镀层金属(填“镀层金属”或“镀件”),电镀液是 AgNO3AgNO3溶液。当乙中溶液的pH是12时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 0.540.54,甲中溶液的pH 变小变小(填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为 Fe+Cu2+通电 Cu+Fe2+Fe+Cu2+通电 Cu+Fe2+。
通电
通电
【考点】原电池与电解池的综合.
【答案】正极;颜色变浅;氢氧化铁胶体粒子带正电荷;1:2;镀层金属;AgNO3;0.54;变小;Fe+Cu2+ Cu+Fe2+
通电
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/14 3:0:9组卷:26引用:2难度:0.6