在学习完九年级化学第二单元的知识后,湖南师大附中集团兴趣小组的同学利用课余时间在实验室进行了两个探究课题,请根据已学知识,回答下列问题。
课题一:测定空气中氧气含量的创新实验。
图甲是教材上利用红磷测定空气中氧气含量的实验,小黄同学设计了图乙装置进行改进,夹持装置已省略。
(查阅资料:温度达到40℃时,白磷能燃烧:白磷+氧气点燃五氧化二磷)

步骤1:如图乙,连接装置,首先检查装置的 气密性气密性;
步骤2:装入相关药品,调节左右两边玻璃管内的水面相平,测得左侧玻璃管内气体的体积为V1mL;
步骤3:关闭弹簧夹,用酒精灯加热铜丝引燃白磷,待火焰熄灭后,过一段时间打开弹簧夹,观察到左侧管内水位上升,待水位不再上升时,测得左侧玻璃管内气体的体积为V2mL;
步骤4:再向右侧容器内加入一定量的水至两侧水面再次相平,测得左侧玻璃管内气体的体积为V3mL。
(1)该实验改进后的突出优点有 环保,结果更准确环保,结果更准确(写2点)。
(2)通过上述实验,小黄同学测得装置中氧气的体积分数为 V1-V3V1V1-V3V1×100%。
课题二:探究过氧化氢溶液分解生成氧气的速率的影响因素。
小唐同学利用实验室的相关仪器与药品,设计如下实验:
点燃
V
1
-
V
3
V
1
V
1
-
V
3
V
1
| 实验序号 | 过氧化氢溶液浓度 | 过氧化氢溶液体积/mL | 温度/℃ | 二氧化锰用量/g | 氧气体积/mL | 反应所需时间/s |
| ① | 5% | 20 | 20 | 0 | 100 | t1 |
| ② | 5% | 20 | 20 | 0.2 | 100 | t2 |
| ③ | 10% | 20 | 20 | 0.2 | 100 | t3 |
| ④ | 15% | 20 | 30 | 0.2 | 100 | t4 |
| ⑤ | 15% | 20 | 50 | 0.2 | 100 | t5 |
过氧化氢溶液浓度、温度、二氧化锰
过氧化氢溶液浓度、温度、二氧化锰
。(4)该实验中小唐同学利用了图丙装置测氧气体积,图丙方框中的装置可选择图丁中的
C
C
(填字母,图中箭头代表物质的流动方向,忽略氧气在水中的溶解)。(5)对比实验④⑤,若t4>t5,可以得出实验结论:在其他条件相同的情况下,
温度越高,反应越快
温度越高,反应越快
。【考点】测定空气里氧气含量的探究.
【答案】气密性;环保,结果更准确;;过氧化氢溶液浓度、温度、二氧化锰;C;温度越高,反应越快
V
1
-
V
3
V
1
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/28 20:0:2组卷:71引用:1难度:0.5
相似题
-
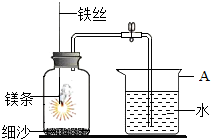 1.某校研究性学习小组用如图所示装置进行镁条在空气中燃烧的实验。待镁条完全燃烧并冷却后打开弹簧夹,进入集气瓶中水的体积约占集气瓶容积的70%。
1.某校研究性学习小组用如图所示装置进行镁条在空气中燃烧的实验。待镁条完全燃烧并冷却后打开弹簧夹,进入集气瓶中水的体积约占集气瓶容积的70%。
(1)图中A仪器的名称是。镁条燃烧并冷却后打开弹簧夹,水能进入到集气瓶中的原因是。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
【发现问题】氮气是如何减少的?
【做出猜想】。
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化化镁中氮的化合价是。镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,反应的化学方程式为2Mg+CO2C+2MgO,该反应所的基本反应类型是点燃。
(3)通过以上探究,你对燃烧的有关知识有了哪些新的认识?(写出一条即可)
(4)24g镁在二氧化碳中燃烧可生成多少克氧化镁?发布:2024/11/18 8:0:1组卷:13引用:1难度:0.5 -
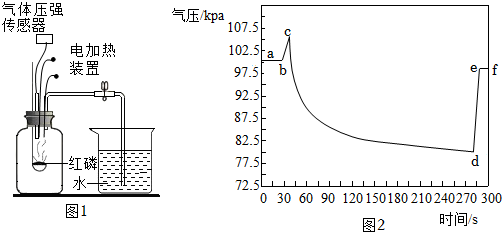
2.如图1是某化学兴趣小组利用气压传感器测定红磷燃烧时集气瓶内气压变化的实验装置。图2是集气瓶内气压随时间的变化情况。下列说法不正确的是( )
 发布:2024/12/25 11:30:2组卷:1085引用:3难度:0.7
发布:2024/12/25 11:30:2组卷:1085引用:3难度:0.7 -
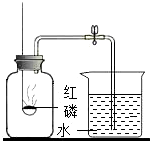 3.测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
3.测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
(1)实验时,取下橡胶塞,点燃红磷后迅速伸入集气瓶中并旋紧橡胶塞,这时看到的现象是,该反应的文字表达式为。
(2)甲同学:用足量的木炭代替红磷做测定空气中氧气含量的实验,结果实验失败了,请你帮助他分析失败的原因:。
(3)乙同学:想用镁条来代替红磷做实验,老师告诉他这种方法不是较好的方法,因为镁条在空气中燃烧非常剧烈,镁既可以和氧气反应,也可以和氮气反应生成氮化镁。请写出镁和氮气反应生成氮化镁的文字表达式:。
(4)丙同学:打算用铁丝替代红磷,实验能否成功?请说明理由。。
(5)燃烧后,集气瓶内剩余的气体主要是氮气,请结合本实验推测氮气的物理性质是。发布:2024/11/7 8:0:2组卷:19引用:1难度:0.5


