丁烷的催化裂解可按下列两种方式进行:C4H10→C2H6+C2H4;C4H10→CH4+C3H6;某化学兴趣小组的同学为探究丁烷裂解气中CH4和C2H6的比例关系,设计如图所示实验:
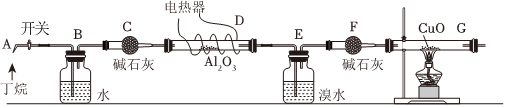
注:CuO能将烃氧化成CO2和H2O;Al2O3是丁烷裂解的催化剂,G后面装置已省略。如图连接好装置后(部分夹持装置已略去),需进行的实验操作有:①给D、G装置加热:②检查整套装置的气密性;③排尽装置中的空气。
(1)这三步操作的先后顺序依次是 ②③①②③①。
(2)简要说明检验空气排尽的方法:用一小试管收集从G装置右端导管口逸出的气体,点燃检验其纯度,若已纯净,则空气排尽用一小试管收集从G装置右端导管口逸出的气体,点燃检验其纯度,若已纯净,则空气排尽。
(3)B装置所起的作用是 通过观察气泡,控制气体流量(或控制气体流速)通过观察气泡,控制气体流量(或控制气体流速)。
(4)F装置所起的作用是 吸收溴蒸气和水吸收溴蒸气和水。
(5)假设丁烷完全裂解,流经各装置中的气体能完全反应。当E和F装置的总质量比反应前增加了4.9g,G装置中固体质量减少了14.4g,则丁烷的裂解产物n(CH4):n(C2H6)=2:12:1。
(6)若对E装置中的混合物再按以下流程实验:

①分离操作Ⅰ、Ⅱ的名称是Ⅰ分液分液、Ⅱ蒸馏蒸馏;
②Na2SO3溶液的作用是(用离子方程式表示) SO2-3+Br2+H2O=SO2-4+2Br-+2H+SO2-3+Br2+H2O=SO2-4+2Br-+2H+。
SO
2
-
3
SO
2
-
4
SO
2
-
3
SO
2
-
4
【考点】探究石蜡油分解制乙烯及乙烯的化学性质.
【答案】②③①;用一小试管收集从G装置右端导管口逸出的气体,点燃检验其纯度,若已纯净,则空气排尽;通过观察气泡,控制气体流量(或控制气体流速);吸收溴蒸气和水;2:1;分液;蒸馏;+Br2+H2O=+2Br-+2H+
SO
2
-
3
SO
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/6 8:0:9组卷:111引用:1难度:0.6
相似题
-
1.实验室中用如图所示装置模拟工业上用石蜡油分解制乙烯。下列关于该实验的说法不正确的是( )
 发布:2024/11/22 8:0:1组卷:79引用:1难度:0.6
发布:2024/11/22 8:0:1组卷:79引用:1难度:0.6 -
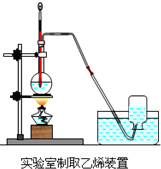 2.乙烯的实验室制法:
2.乙烯的实验室制法:
(1)药品:、
(2)反应原理:(方程式)
(3)在圆底烧瓶中放入少量碎瓷片是为了防止液体发生
(4)反应中浓硫酸的作用、
(5)将乙烯通入酸性高锰酸钾溶液中,现象是其反应类型是;
(6)将乙烯通入溴水中,现象是,所发生的化学反应方程式其反应类型是.发布:2024/10/26 17:0:2组卷:155引用:1难度:0.5 -
 3.1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189.cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷.
3.1,2二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.189.cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可用下列反应制备1,2二溴乙烷.
①CH3CH2OHCH2═CH2↑+H2OH2SO4△
②CH2═CH2+Br2→CH2BrCH2Br
某化学兴趣小组用如图1所示的装置(部分固定和夹持装置省略)进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色.
回答下列问题:
(1)已知该实验的副反应之一是乙醇会被浓硫酸氧化成CO2.写出该反应的化学方程式:.
(2)甲同学认为:溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由是(填正确答案的标号,下同).
A.乙烯与溴水易发生取代反应 B.使溴水褪色的物质,未必是乙烯
C.使溴水褪色的反应,未必是加成反应
D.浓硫酸氧化乙醇生成的乙醛,也会使溴水褪色
(3)乙同学经过仔细观察后认为试管中另一现象可证明反应中有乙烯生成,该现象是.
(4)丙同学对上述实验进行了改进,在Ⅰ和Ⅱ之间增加如图2所示的装置,则A中的试剂为,其作用是,B中的试剂为,其作用是.
(5)丁同学通过洗涤、蒸馏等操作对1,2一二溴乙烷粗品进行了精制.该洗涤操作用到的主要玻璃仪器是,该仪器在使用前须清洗干净并.发布:2024/11/7 8:0:2组卷:449引用:1难度:0.5


