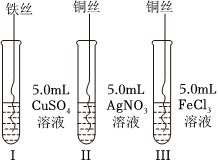
为了探究Fe3+、Fe2+、Cu2+、Ag+的氧化性强弱,设计实验如图所示。请回答:
(1)写出AgNO3的电离方程式:AgNO3=Ag++NO-3AgNO3=Ag++NO-3。
(2)实验Ⅰ、Ⅱ的现象和结论如表:
N
O
-
3
N
O
-
3
| 实验编号 | 实验现象 | 实验结论 |
| Ⅰ | ① | 氧化性:Cu2+>Fe2+ |
| Ⅱ | 溶液变蓝色 | ② |
| Ⅲ | 铜丝溶解,溶液颜色变浅 | 氧化性:Fe3+>Cu2+ |
铁丝上有红色固体析出
铁丝上有红色固体析出
。②实验Ⅱ的结论
氧化性:Ag+>Cu2+
氧化性:Ag+>Cu2+
。③写出实验Ⅱ中发生反应的离子方程式:
Cu+2Ag+=Cu2++2Ag
Cu+2Ag+=Cu2++2Ag
。④写出实验Ⅲ中发生反应的离子方程式:
Cu+2Fe3+=2Fe2++Cu2+
Cu+2Fe3+=2Fe2++Cu2+
。(3)Fe、Cu、CuSO4溶液、AgNO3溶液均能导电,CuSO4溶液、AgNO3溶液能导电的原因是
CuSO4、AgNO3能电离出自由移动的离子
CuSO4、AgNO3能电离出自由移动的离子
。(4)实验Ⅱ中的AgNO3完全反应后,抽出铜丝,洗净后干燥,称重,发现铜丝比反应前增重0.152g,则反应生成的Ag的质量为
0.216
0.216
g。【考点】氧化性、还原性强弱的比较.
【答案】AgNO3=Ag++;铁丝上有红色固体析出;氧化性:Ag+>Cu2+;Cu+2Ag+=Cu2++2Ag;Cu+2Fe3+=2Fe2++Cu2+;CuSO4、AgNO3能电离出自由移动的离子;0.216
N
O
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/23 3:0:1组卷:50引用:2难度:0.5
相似题
-
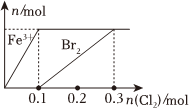 1.向200mLFeBr2溶液中逐渐通入Cl2,其中n(Fe3+)、n(Br2 )随通入n(Cl2)的变化如图所示,下列说法错误的是( )发布:2024/12/7 9:30:1组卷:50引用:3难度:0.5
1.向200mLFeBr2溶液中逐渐通入Cl2,其中n(Fe3+)、n(Br2 )随通入n(Cl2)的变化如图所示,下列说法错误的是( )发布:2024/12/7 9:30:1组卷:50引用:3难度:0.5 -
2.根据反应式:①2Fe3++2I-═2Fe2++I2,②Br2+2Fe2+═2Br-+2Fe3+,可判断离子的还原性从强到弱的顺序是( )
发布:2024/11/28 12:30:2组卷:346引用:8难度:0.8 -
3.已知:
①2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O;
②Cl2+2FeCl2═2FeCl3;
③2KI+2FeCl3═2KCl+I2+2FeCl2。
则下列判断正确的是( )发布:2024/12/11 14:0:2组卷:421引用:7难度:0.4


