 根据中和滴定原理,用0.1125mol/LHCl溶液测定未知浓度NaOH溶液的浓度。
根据中和滴定原理,用0.1125mol/LHCl溶液测定未知浓度NaOH溶液的浓度。
(1)滴定准备:
从下列选项中选择合理的操作并排序(用字母表示,操作不能重复使用):选取外观完好的滴定管→用自来水洗净→检查滴定管是否漏水→( bb)→( aa)→( dd)→( ee)→( cc)。
a.用待装液润洗2~3次
b.用蒸馏水洗涤
c.调节管内液面于“0”刻度或“0”刻度以下
d.加入待装液使液面位于滴定管“0”刻度以上2~3mL处
e.排出滴定管尖嘴部分的气泡
(2)滴定过程:
①从碱式滴定管中放出待测NaOH溶液25.00mL于锥形瓶中,滴加 BB作指示剂。
A.2滴石蕊溶液
B.2滴酚酞溶液
C.1mL石蕊溶液
D.1mL酚酞溶液
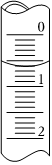
②若酸式滴定管中HCl溶液液面位置如图所示,读数为 0.600.60mL。
③用HCl溶液滴定至终点,达到滴定终点的判断依据是 滴入最后半滴HCl溶液后,溶液由粉红色刚好变为无色,且半分钟内不变色滴入最后半滴HCl溶液后,溶液由粉红色刚好变为无色,且半分钟内不变色。
(3)数据处理:
| 实验编号 | NaOH待测液体积V/mL | 消耗HCl标准液体积V/mLL |
| 1 | 25.00 | 22.60 |
| 2 | 25.00 | 24.00 |
| 3 | 25.00 | 23.98 |
| 4 | 25.00 | 24.02 |
0.1080
0.1080
mol/L(计算结果保留4位有效数字)。(4)误差分析:
以下操作会导致待测NaOH溶液浓度测定结果偏高的是
BC
BC
。A.装入待测液前,锥形瓶中有少量水
B.锥形瓶洗净后,用待测液润洗2~3次
C.用碱式滴定管量取NaOH溶液,开始时尖嘴部分无气泡,放液结束出现气泡
D.滴定过程中振荡锥形瓶时部分NaOH溶液溅出
E.装HCl溶液的滴定管,滴定前读数时仰视,滴定后读数时俯视
(5)实验反思:
在氧化还原滴定实验中,盛装高锰酸钾溶液可选用
AC
AC
。A.酸式滴定管
B.碱式滴定管
C.使用聚四氟乙烯活塞的滴定管
【考点】中和滴定.
【答案】b;a;d;e;c;B;0.60;滴入最后半滴HCl溶液后,溶液由粉红色刚好变为无色,且半分钟内不变色;0.1080;BC;AC
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/2 8:0:9组卷:76引用:1难度:0.6
相似题
-
1.下列实验方法或操作正确的是( )
发布:2024/12/12 8:0:1组卷:9引用:1难度:0.7 -
2.下面关于中和滴定的实验操作叙述不正确的有( )
①将锥形瓶用蒸馏水和待测定的盐酸溶液进行洗涤
②取20mL待测定的盐酸溶液,注入锥形瓶中
③向锥形瓶中加入几滴酚酞试液为指示剂
④碱式滴定管用蒸馏水洗涤后,直接注入已知浓度的NaOH溶液
⑤进行中和滴定时,一旦锥形瓶内溶液由无色变成粉红色,即可停止滴定
⑥记录数据,进行必要的数据处理和得出结论发布:2024/12/10 0:30:1组卷:94引用:2难度:0.7 -
3.食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL,实验室用标准NaOH溶液测定食醋中醋酸的浓度,以检测食醋是否符合国家标准,某品牌白醋的醋酸浓度测定过程如图所示,请回答:
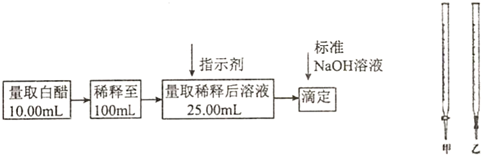
(1)选用上述(填“甲”或“乙”)滴定管量取10.00mL白醋后,将白醋稀释至100mL时,需要使用的玻璃仪器有烧杯、玻璃棒和.
(2)某同学用酸碱中和滴定法测定该品牌白醋的醋酸浓度,当醋酸与氢氧化钠恰好完全反应时,测得溶液中=c(CH3COOH)c(CH3COO-),则此时溶液中的pH=11.8×103.(已知:室温下醋酸的Ka=1.8×10-5)
(3)根据该同学的计算结果,应该选作指示剂.(填“酚酞”、“甲基橙”或“石蕊”)
(4)该滴定达到终点时的现象是.
(5)某次实验滴定开始和结束时,碱式滴定管中的液面如下图所示,则所用NaOH溶液的体积为mL.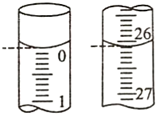
(6)用标准的0.06000mol⋅L-1NaOH溶液滴定上述稀释后的醋酸溶液,滴定结果如下表所示:
则该品牌白醋中醋酸含量为滴定次数 待测溶液的体积/mL 标准溶液的体积 滴定前刻度/mL 滴定后刻度/mL 1 25.00mL 0.02 25.01 2 25.00mL 0.70 25.71 3 25.00mL 0.50 24.2 mg/mL.
(7)下列操作中,可能使所测白醋中醋酸的浓度数值偏高的是.(填编号)
A.取待测液的滴管,取液前滴定管尖嘴处无气泡,取液后尖嘴处出现气泡
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
D.读取NaOH溶液体积时,开始时俯视读数,滴定结束时仰视读数
(8)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10.00mL刻度处,现把管内液体全部放出,用量筒接收,得到溶液的体积是.
A.等于10mL
B.等于40mL
C.大于40mL
D.不能确定发布:2024/12/30 3:0:4组卷:54引用:2难度:0.6


