学习酸的性质是一项重要的内容,某化学兴趣小组以“探究硫酸的性质”为主题开展项目式学习。请回答下列问题。
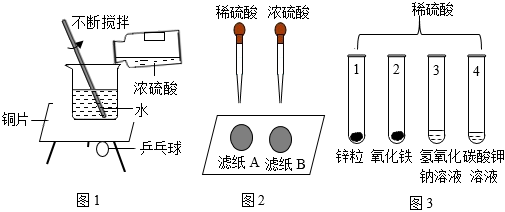
【任务一】浓硫酸稀释过程中的能量变化。
图1实验中,观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水 放热放热(填“放热”或“吸热”)。
【任务二】硫酸的浓度对硫酸化学性质的影响。
图2实验中,观察到很快变黑的是 滤纸B滤纸B(填“滤纸A”或“滤纸B”),由此可知硫酸的浓度不同,硫酸的腐蚀性不同。
【任务三】稀硫酸的化学性质。
小组同学按图3进行实验,分别将稀硫酸滴加到各个试管中。
(1)试管1中发生反应的化学方程式为 Zn+H2SO4=ZnSO4+H2↑Zn+H2SO4=ZnSO4+H2↑。
(2)试管2中可观察到的现象是 红棕色固体逐渐溶解,溶液由无色变成黄色红棕色固体逐渐溶解,溶液由无色变成黄色。
(3)该小组同学利用数字化传感器测得试管3中不断滴加稀硫酸时溶液pH的变化图像如图4所示,硫酸和氢氧化钠恰好完全反应的微观示意图如图5所示。
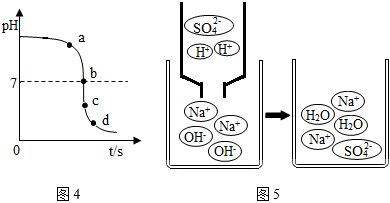
①图4中a点所示溶液中含有的溶质是 NaOH、Na2SO4NaOH、Na2SO4(填化学式)。
②该反应的微观实质是 氢离子和氢氧根离子结合生成水分子氢离子和氢氧根离子结合生成水分子。
(4)小组同学对试管4中反应后的溶质成分产生了兴趣,他们继续进行实验。
【提出问题】试管4中反应后的溶液中溶质成分是什么?
【作出猜想】猜想一:可能是K2SO4;
猜想二:可能是 K2SO4、K2CO3K2SO4、K2CO3(填化学式);
猜想三:可能是K2SO4、H2SO4。
【实验与结论】某同学用洁净干燥的玻璃棒蘸取试管4中反应后的溶液滴到湿润的pH试纸上,测得pH=4,他认为猜想三正确。
【反思与评价】对该同学的操作方法、测量结果及结论进行评价,正确的是 CC(填字母)。
A.方法不正确,结果偏小,结论正确
B.方法正确,结果偏大,结论不正确
C.方法不正确,结果偏大,结论正确
D.方法正确,结果偏小,结论不正确
【任务四】废液回收处理。
实验结束后在老师指导下,同学们将四支试管中的液体倒入废液缸,并对废液缸中的固体物质进行了回收。在检验废液时发现硫酸过量,为防止其污染环境,从实验成本的角度考虑,应向该废液中加入适量的 熟石灰熟石灰(填物质名称),处理后再排放。
【答案】放热;滤纸B;Zn+H2SO4=ZnSO4+H2↑;红棕色固体逐渐溶解,溶液由无色变成黄色;NaOH、Na2SO4;氢离子和氢氧根离子结合生成水分子;K2SO4、K2CO3;C;熟石灰
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/27 10:35:59组卷:117引用:4难度:0.6
相似题
-
1.(1)将一枚表面生锈的铁钉足量的稀盐酸中,可以观察到得现象是
,溶液颜色呈,发生的化学反应方程式为:;过一段时间后可以看到铁钉表面,此时发生反应的化学方程式为;
(2)A、B两支试管中分别盛有少量的稀盐酸和稀硫酸,然后向两支试管中分别滴加硝酸钡(Ba(NO3)2 )溶液,可以观察到得现象是:A试管中,B试管中,所发生反应的化学方程式为.发布:2024/12/25 17:0:2组卷:62引用:2难度:0.5 -
2.下列四种物质中,其中有一种物质能和其他三种物质发生反应,该物质是( )
发布:2024/12/25 17:0:2组卷:69引用:4难度:0.7 -
3.把一颗生锈的铁钉放入足量的稀盐酸中,先看到的现象是
.写出该反应的化学方程式.过一会儿,又看到的现象是.其反应方程式为.发布:2024/12/25 17:30:2组卷:47引用:2难度:0.9


