当前位置:
试题详情
二氧化硫是一种危害严重的大气污染物,烟气脱硫是控制二氧化硫污染的主要技术手段。
利用海水脱硫是一种有效的方法,其工艺流程如图1所示。
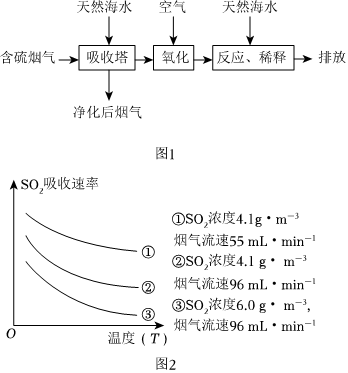
某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验。实验结果如图2所示。
(1)根据图示2实验结果,为了提高一定浓度含硫烟气中SO2的吸收效率,下列措施正确的是 ABDABD(填字母)。
A.降低通入含硫烟气的温度
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
D.在天然海水中加入生石灰
(2)天然海水吸收了含硫烟气后会溶有H2SO3,使用空气中的氧气将其氧化,写出该反应的离子方程式:2H2SO3+O2=4H++2SO2-42H2SO3+O2=4H++2SO2-4。
(3)该小组采用如图装置在实验室测定烟气中SO2的体积分数(假设烟气中其余组分不能与水反应且不溶于水,实验在标准状况下进行):
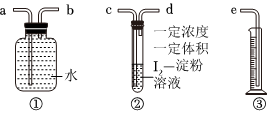
①上述装置连接的正确顺序是:原料气→cc→dd→bb→aa→ee。(填a、b、c、d、e)
②下列试剂中(浓度、体积一定),可以用来代替试管中的I2-淀粉溶液的是 ACAC(填字母)。
A.酸性KMnO4溶液
B.NaOH溶液
C.溴水
D.氨水
SO
2
-
4
SO
2
-
4
【考点】二氧化硫的污染及治理.
【答案】ABD;2H2SO3+O2=4H++2;c;d;b;a;e;AC
SO
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/25 8:0:9组卷:4引用:1难度:0.5
相似题
-
1.利用石灰石和烟气中的SO2反应生成石膏,可实现烟气中脱除SO2。某研究性学习小组在实验室利用如图所示装置制备烟气(主要成分为SO2、CO2、N2、O2),并测定烟气中SO2的体积分数以及研究烟气通过转化器的脱硫效率。请回答下列问题:
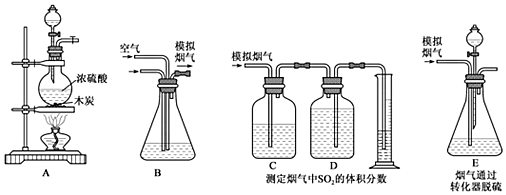
Ⅰ.模拟烟气的制备。
(1)装置A中发生反应的化学方程式:。
Ⅱ.测定烟气中SO2的体积分数。
(2)将A中产生的气体与空气一起通过B装置混合均匀,从而形成模拟烟气。将部分模拟烟气缓慢通过C、D装置,其中C、D中盛有的药品分别是、。(填序号)
a.KMnO4溶液
b.饱和NaHSO3溶液
c.饱和Na2CO3溶液
d.饱和NaHCO3溶液
装置C的作用是:。
(3)①甲同学认为测定烟气中SO2的体积分数的装置中存在缺陷,你觉得应如何改进。
②乙同学根据模拟烟气的流速amL•min-1和t1min后测得的量筒内液体的体积VmL,计算烟气中二氧化硫的体积分数是。
Ⅲ.模拟烟气通过转化器的脱硫效率研究。
(4)E中溶液可以催化SO2与O2的反应生成SO42-,以达到脱硫的目的。若模拟烟气仍以amL•min-1的流速通过转化器E装置,t2min后,向E装置中加入酸化的BaCl2溶液,得到白色浑浊液,经过滤、洗涤、干燥、称量,得到mg固体。若实验测得的气体体积已折算为标准状况下的体积,则该转化器的脱硫效率是。发布:2024/12/30 4:30:1组卷:80引用:2难度:0.6 -
2.认识含硫物质的性质及转化规律,能帮助我们更好地认识自然和保护环境。
(1)酸雨的形成原因,将SO2气体通入蒸馏水中,取出部分溶液并用pH计测定其pH,每隔 10min读数一次,所得数据如下:
随着时间的推移,pH逐渐变小的原因是时间(min) 0 10 20 30 40 pH 4.95 4.94 4.86 4.85 4.85 (用化学方程式表示)。
(2)防治SO2对环境的污染。
①从物质分类角度看,SO2属于酸性氧化物,工业上常用熟石灰将SO2转化为亚硫酸盐,写出所得亚硫酸盐的化学式:。
②从元素价态看,SO2中S元素为+4价,既具有氧化性,又具有还原性。用生物质热解气(主要成分为CO、CH4、H2)可将SO2在高温下还原成单质硫。写出CO还原SO2反应的化学方程式:。
(3)获取空气质量信息。某化学小组为了测定空气中SO2的体积分数,做了如下实验:取标准状况下的空气20.00L(含N2、O2、CO2、SO2),缓慢通过足量溴水,反应的化学方程式为:SO2+Br2+H2O→2HBr+H2SO4。在所得溶液中加入稍过量的BaCl2溶液,产生白色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为4.66g。空气样品中SO2的体积分数为。
(4)你认为减少酸雨可采取的措施是(填字母)。①少用煤作燃料②把工厂烟囱造高③化石燃料脱硫④在已酸化的土壤中加生石灰⑤开发新能源
A.①②③
B.②③④⑤
C.①③⑤
D.①③④⑤发布:2024/12/30 5:0:1组卷:61引用:3难度:0.8 -
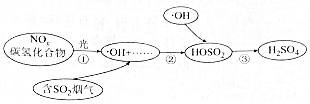 3.研究表明,硫酸型酸雨的形成与空气中氮的氧化物和碳氢化合物有关,其部分过程如图所示。下列说法错误的是( )发布:2024/12/30 7:0:1组卷:3引用:1难度:0.7
3.研究表明,硫酸型酸雨的形成与空气中氮的氧化物和碳氢化合物有关,其部分过程如图所示。下列说法错误的是( )发布:2024/12/30 7:0:1组卷:3引用:1难度:0.7


