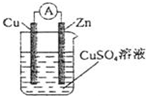
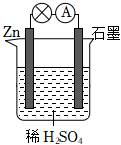
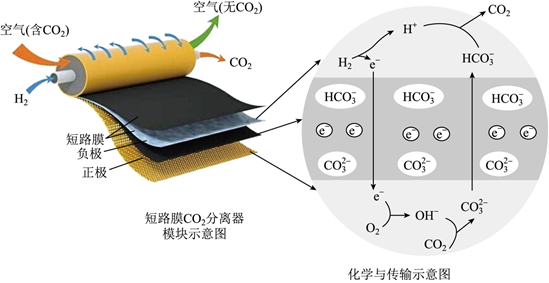
通过电解ZnSO4、MnSO4的混合溶液得到普通干电池中的锌与MnO2,某研究小组设计了如图所示的实验探究装置。

回答下列问题:
(1)燃料电池的优点是 能量转化率高,环境友好能量转化率高,环境友好,图中是将两个甲烷燃料电池串联后作为电源,负极的电极反应为 CH4+10OH--8e-=CO2-3+7H2OCH4+10OH--8e-=CO2-3+7H2O。
(2)闭合开关K后,铝电极上的产物是 锌锌,一段时间后阳极附近溶液的pH 减小减小(填“增大”、“不变”或“减小”),电解ZnSO4、MnSO4的混合溶液的阳极反应式为 Mn2+-2e-+2H2O=MnO2+4H+Mn2+-2e-+2H2O=MnO2+4H+。
(3)假定燃料电池中的化学能完全转化为电能,负极每消耗2.24L(标准状况)CH4,电解池中回收制得19.5g单质Zn,电解池的能量利用率为 75%75%。
CO
2
-
3
CO
2
-
3
【考点】原电池与电解池的综合.
【答案】能量转化率高,环境友好;CH4+10OH--8e-=+7H2O;锌;减小;Mn2+-2e-+2H2O=MnO2+4H+;75%
CO
2
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/9/13 16:0:8组卷:2引用:2难度:0.5