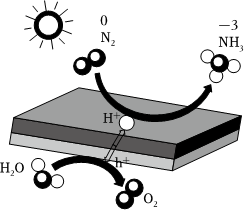
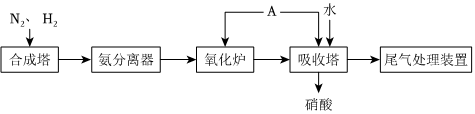
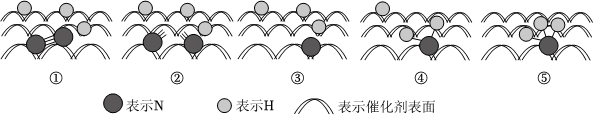
工业上通过氮气和氢气反应合成氨,氨经一系列反应可以得到硝酸。反应如图所示:

请回答:
(1)下列说法不正确的是 dd(填序号字母)。
a.氮气可用作保护气
b.铵态氮肥一般不能与碱性化肥共同使用
c.硝酸可用于制化肥、农药、炸药、染料、盐类等
d.某浓硝酸中含有溶质2mol,该浓硝酸与足量铜反应最多可生成1molNO2
(2)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大。
①合成氨反应中的能量变化如图所示,该反应是 放热放热反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量 小于小于(填“大于”或“小于”)生成物化学键形成放出的总能量。
②在一定条件下,将一定量N2和H2的混合气体充入某恒容密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是 cc(填序号字母)。

a.容器中N2、H2、NH3共存
b.N2、H2、NH3的物质的量之比为1:3:2
c.容器中的压强不随时间变化
d.N2、NH3浓度相等
(3)工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
①水吸收法。用化学方程式说明用水吸收NO2的缺陷 3NO2+H2O=2HNO3+NO3NO2+H2O=2HNO3+NO。
②NaOH溶液吸收法。发生的反应有:2NaOH+NO+NO2→2NaNO2+H2O
22NaOH+22NO2=NaNO3NaNO3+11NaNO2+11H2O(填化学式,并配平方程式)。
③用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:(α表示尾气里NO、NO2中NO2的含量)

i.根据图得知 bb(填序号字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.NO2含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入H2O2能提升氮氧化物的吸收率,原因是 H2O2具有氧化性,能将NO氧化成NO2,NO2含量增大,氮氧化物吸收率提升H2O2具有氧化性,能将NO氧化成NO2,NO2含量增大,氮氧化物吸收率提升。
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来。请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+;以“ ”代表反应容器,“
”代表反应容器,“ ”代表导线,“
”代表导线,“ ”代表电极,“
”代表电极,“ ”代表小灯泡,在如图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极
”代表小灯泡,在如图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极 
 。
。


【答案】d;放热;小于;c;3NO2+H2O=2HNO3+NO;2;2;NaNO3;1;1;b;H2O2具有氧化性,能将NO氧化成NO2,NO2含量增大,氮氧化物吸收率提升;

【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/29 8:0:10组卷:26引用:1难度:0.7