煤是重要的能源,也是生产化工产品的重要原料。随着人类社会的飞速发展,化石能源大量消耗,人类已经面临较严重的能源危机。为此,提高能源的利用率和开发更多的新能源显得相当重要。如图是煤化工产业链的一部分。
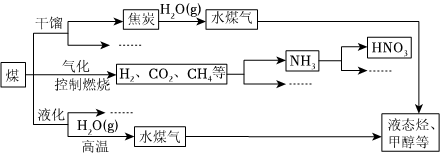
请回答:
(1)任意列举两项新能源 太阳能、生物质能或氢能、风能等太阳能、生物质能或氢能、风能等。
(2)上述处理煤的过程属于 化学化学(填“物理”或“化学”)变化。
(3)煤和石油等化石燃料燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通入含有长石(地壳中最常见的矿石,含量高达60%)成分的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,则X的名称是 氢氧化铝氢氧化铝。
(4)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如图所示:
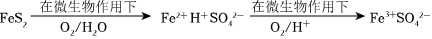
这种脱硫技术称为微生物脱硫技术。该技术的两步反应的化学方程式依次是 2FeS2+7O2+2H2O 微生物 4H++2Fe2++4SO2-4、4Fe2++O2+4H+ 微生物 4Fe3++2H2O2FeS2+7O2+2H2O 微生物 4H++2Fe2++4SO2-4、4Fe2++O2+4H+ 微生物 4Fe3++2H2O。
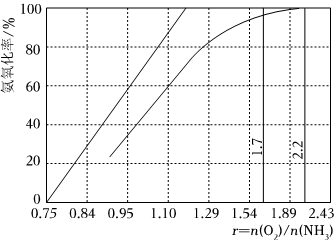
(5)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ[n(O2)n(NH3)]=1.25,实际生产要将γ值维护在1.7~2.2之间,原因是 O2浓度太少不利于NH3的转化,γ[n(O2)n(NH3)]值为2.2时NH3氧化率已近100%O2浓度太少不利于NH3的转化,γ[n(O2)n(NH3)]值为2.2时NH3氧化率已近100%。[温馨提示:n(O2)是可以认为是表示氧气分子堆积数目的一种物理量,即n(O2)值越大,说明氧分子数目越多]
微生物
SO
2
-
4
微生物
微生物
SO
2
-
4
微生物
n
(
O
2
)
n
(
N
H
3
)
n
(
O
2
)
n
(
N
H
3
)
n
(
O
2
)
n
(
N
H
3
)
【答案】太阳能、生物质能或氢能、风能等;化学;氢氧化铝;2FeS2+7O2+2H2O 4H++2Fe2++4、4Fe2++O2+4H+ 4Fe3++2H2O;O2浓度太少不利于NH3的转化,γ[]值为2.2时NH3氧化率已近100%
微生物
SO
2
-
4
微生物
n
(
O
2
)
n
(
N
H
3
)
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/31 8:0:9组卷:42引用:1难度:0.6


