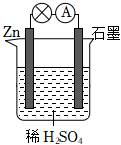
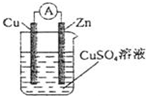
如图所示装置中,甲、乙两个烧杯分别依次盛放200mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16g.据此回答问题:
如图所示装置中,甲、乙两个烧杯分别依次盛放200mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16g.据此回答问题:
(1)电源的N端为 负负极;
(2)电极b上发生的电极反应为 2H++2e‑=H2↑2H++2e‑=H2↑;
(3)电极c上生成的气体在标准状态下的体积:0.112L0.112L;
(4)甲溶液的pH为 1313(设溶液体积仍为200mL);
(5)欲在丙烧杯中实现铁的表面镀上一层锌,则电解质溶液为 ZnCl2ZnCl2,e电极的材料是:ZnZn,f电极的电极反应式为 Zn2++2e-=ZnZn2++2e-=Zn.
【考点】原电池与电解池的综合.
【答案】负;2H++2e‑=H2↑;0.112L;13;ZnCl2;Zn;Zn2++2e-=Zn
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/17 22:0:1组卷:25引用:4难度:0.3