(1)用下面的原子或者离子结构示意图的编号(A、B、C和D)填空:
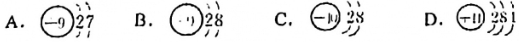
①电子层排布相同的是 BCBC;
②属于同种元素的是 ABAB。
③属于金属元素的是 DD;
④属于稀有气体元素的是 CC。
(2)写出表示含有8个质子,10个中子的原子的化学符号: 188O 188O画出其原子结构示意图 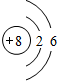
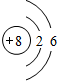 。
。
(3)在离子ROn-3中,共有x个核外电子,R原子的质量数为A,则R含有的中子数是 A-x+n+24A-x+n+24。
(4)相同物质的量的14CO2与S18O2的质量之比为 23:2623:26;中子数之比为 2:32:3。
(5)2L硫酸铝溶液中含2.7gAl3+,则该溶液中SO2-4的物质的量浓度是 0.075mol/L0.075mol/L。
18
8
18
8
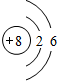
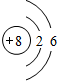
RO
n
-
3
SO
2
-
4
【考点】物质的量的相关计算;原子结构示意图、离子结构示意图.
【答案】BC;AB;D;C; O;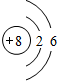 ;A-x+n+24;23:26;2:3;0.075mol/L
;A-x+n+24;23:26;2:3;0.075mol/L
18
8
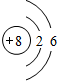 ;A-x+n+24;23:26;2:3;0.075mol/L
;A-x+n+24;23:26;2:3;0.075mol/L【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/17 13:0:1组卷:12引用:2难度:0.7
相似题
-
1.(1)0.5mol CO2约含有
个CO2分子,mol O原子;
(2)1.204×1023个CH4分子中含有mol C原子,约含有个H原子;
(3)0.25mol Na2SO4含有mol Na+,mol SO42-,约含有个O.发布:2024/12/30 18:30:1组卷:11引用:1难度:0.9 -
2.已知某元素的阳离子R2+的核内中子数为N,质量数为A,则1mol它的氧化物中所含电子的物质的量是( )
发布:2024/12/30 14:30:1组卷:20引用:4难度:0.6 -
3.回答下列问题。
(1)49gH2SO4中氧原子数为。
(2)16g物质A中含有的分子数为3.01×1023,则A的摩尔质量为。
(3)在标准状况下,1.7gNH3与标准状况下LH2S含有相同数目的氢原子。
(4)0.17gOH-中质子的物质的量为,电子的微粒数为个。
(5)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的分子数为。
(6)从400mL2.0mol•L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中的物质的量浓度为SO2-4。
(7)标准状况下,等质量的氧气与臭氧的体积之比为,氧原子个数之比为。
(8)同温同压下,容器A中充满CO2气体,容器B中充满N2,若V(A):V(B)=3:2,则两容器中的气体密度比为。发布:2024/12/30 17:0:2组卷:153引用:5难度:0.5


