学习了MnO2对过氧化氢分解有催化作用的知识后,凯米思趣化学社团的同学对红砖粉末是否可以作H2O2分解的催化剂。设计了以下探究实验:
【提出猜想】红砖粉末可以作过氧化氢分解的催化剂。
【实验验证】
| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验一 | 在试管中加入10mL5%的H2O2溶液,然后将带火星的木条伸入试管 | 有少量气泡产生,木条不复燃 | H2O2溶液分解速率较慢 |
| 实验二 | 将10mL5%的H2O2溶液加入装有0.5g红砖粉末的试管,然后将带火星的木条伸入试管中 | 有较多气泡产生,木条复燃 | |
| 实验三 | 将实验二中反应后的混合物过滤、洗涤、干燥、称重 | 固体质量为0.5g | 红砖粉末的质量不变 |
为了证明H2O2分解生成O2的速率较为缓慢
为了证明H2O2分解生成O2的速率较为缓慢
。【讨论与反思】
(2)实验二可得出的实验结论是:
红砖粉末可以加快H2O2溶液分解速率
红砖粉末可以加快H2O2溶液分解速率
。有同学认为上述实验不能证明红砖粉末是过氧化氢分解的催化剂,还要补充以下实验:(3)探究
实验三中得到的红砖粉末是否继续使H2O2溶液催化分解
实验三中得到的红砖粉末是否继续使H2O2溶液催化分解
【实验步骤】。
(4)将实验三中得到的固体放于试管中,然后向其中加入
10mL5%的H2O2溶液
10mL5%的H2O2溶液
,伸入带火星的木条,木条复燃。【结论】
(5)红砖粉末可作H2O2分解的催化剂,其催化H2O2分解的化学反应方程式为
2H2O2 2H2O+O2↑
红砖粉末
2H2O2 2H2O+O2↑
。红砖粉末
【考点】判断某物质在化学反应中是否做催化剂.
【答案】为了证明H2O2分解生成O2的速率较为缓慢;红砖粉末可以加快H2O2溶液分解速率;实验三中得到的红砖粉末是否继续使H2O2溶液催化分解;10mL5%的H2O2溶液;2H2O2 2H2O+O2↑
红砖粉末
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/30 20:0:8组卷:20引用:6难度:0.5
相似题
-
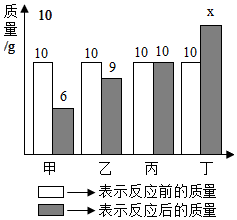 1.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )发布:2024/8/9 8:0:9组卷:54引用:4难度:0.7
1.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )发布:2024/8/9 8:0:9组卷:54引用:4难度:0.7 -
2.在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:
下列说法中,不正确的是( )物质 甲 乙 丙 丁 反应前质量/g 18 1 2 32 反应后质量/g X 26 2 12 发布:2024/8/31 3:0:11组卷:45引用:4难度:0.4 -
3.一定条件下,甲、乙、丙、丁、戊五种物质在密闭容器中发生反应,反应一段时间后,测得反应前后各种物质的质量(单位:g)如图所示,下列说法不正确的是( )
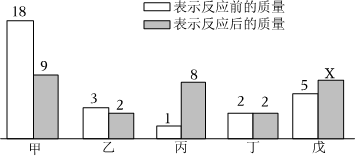 发布:2024/8/3 8:0:9组卷:12引用:1难度:0.5
发布:2024/8/3 8:0:9组卷:12引用:1难度:0.5


