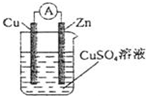
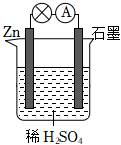
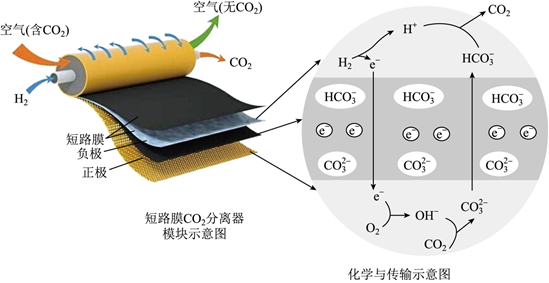
电化学原理在工农业生产中有重要应用。已知N2H4是一种重要的清洁高能燃料,产物无污染。根据如图所示装置回答下列问题(C1~C6均为石墨电极,假设各装置在工作过程中溶液体积不变)。

(1)甲装置C2电极为 正正极,C1电极上的电极反应为 N2H4-4e-+4OH-=N2↑+4H2ON2H4-4e-+4OH-=N2↑+4H2O。
(2)装置中Ag电极上的电极反应为 Ag++e-=AgAg++e-=Ag,若乙装置中溶液体积为400mL,开始时溶液pH为6,当电极上通过0.04mol电子时溶液pH约为 11。
(3)丙装置用于处理含高浓度硫酸钠的废水,同时获得硫酸、烧碱及氢气,膜X为 阴离子阴离子(填“阳离子”“阴离子”或“质子”)交换膜,当电极上通过0.04mol电子时,中间硫酸钠废水的质量改变 2.842.84g(假定水分子不能通过膜X和膜Y)。
(4)电解一段时间后,丁装置中能观察到的现象是 Fe电极逐渐溶解,C6电极上有气泡生成,溶液中出现红褐色沉淀Fe电极逐渐溶解,C6电极上有气泡生成,溶液中出现红褐色沉淀,丁装置中电解反应的总化学方程式为 Fe+2H2O 电解 Fe(OH)2↓+H2↑Fe+2H2O 电解 Fe(OH)2↓+H2↑。
电解
电解
【考点】原电池与电解池的综合;原电池原理.
【答案】正;N2H4-4e-+4OH-=N2↑+4H2O;Ag++e-=Ag;1;阴离子;2.84;Fe电极逐渐溶解,C6电极上有气泡生成,溶液中出现红褐色沉淀;Fe+2H2O Fe(OH)2↓+H2↑
电解
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/14 0:0:2组卷:24引用:1难度:0.6