 梅雨时节,家里常使用“氯化钙除湿剂”除湿防霉,其中悬挂式包装如图所示,一般15天左右,200-300g白色固体全部吸水溶解,收集到的溶液在室温下常有白色晶体析出。
梅雨时节,家里常使用“氯化钙除湿剂”除湿防霉,其中悬挂式包装如图所示,一般15天左右,200-300g白色固体全部吸水溶解,收集到的溶液在室温下常有白色晶体析出。
探究一:收集的溶液中离子成分的鉴定
查阅资料:节日燃放的烟花中加入特定的金属元素,使焰火更加绚丽多彩。在化学上常用焰色反应来测定某种金属元素是否存在于化合物中、用一根洁净的铂丝蘸取样品溶液,再放到酒精灯火焰上,观察焰色。钙、钠、铅的焰色分别是砖红色、黄色和绿色。
实验探究:
(1)
| 编号 | 实验过程 | 实验现象 | 实验结论和解释 |
| 1 | 用洁净的铂丝蘸取收集的溶液,放在酒精灯火 焰上灼烧。 |
火焰呈现 砖红 砖红 色。 |
溶液中含有钙离子。 |
| 2 | 取少量收集的溶液与试管中,加入足量稀硝酸 和少量 硝酸银 硝酸银 溶液。 |
产生白色沉淀。 | 溶液中含有氯离子,反应产生白色沉淀的化学 方程式为 CaCl2+2AgNO3=Ca(NO3)2+2AgCl↓ CaCl2+2AgNO3=Ca(NO3)2+2AgCl↓ 。 |
(2)查阅资料:不同温度下氯化钙的溶解度
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度/g | 59.5 | 64.7 | 74.5 | 100 | 128 | 137 | 147 |
放出
放出
热量,溶液进入集水区后恢复室温,导致晶体析出。请设计实验验证你的猜想 取少量氯化钙固体放入试管中,向试管中加入适量的水,用手触摸试管外壁,感觉温度升高,所以氯化钙溶解是放出热量的
取少量氯化钙固体放入试管中,向试管中加入适量的水,用手触摸试管外壁,感觉温度升高,所以氯化钙溶解是放出热量的
。探究三:渗液处理方法原理的探究
“氯化钙除湿剂”的部分注意事项:
①若不慎渗漏请用小苏打水[小苏打为碳酸氢钠(NaHCO3)]擦拭;
②溶液呈弱碱性,不可浇花或作其它用途,请将液体倒入排水管后丢弃”。
小组同学合作完成下列实验:
(3)测定收集溶液的酸碱度:取少量收集的溶液,用
酸度计或pH计
酸度计或pH计
测出其酸碱度为8.38。(4)配制5%的碳酸氢钠溶液50g
①实验步骤为计算、
称量
称量
、溶解、转移。②溶解时玻璃棒的作用为
搅拌,加速溶解(合理即可)
搅拌,加速溶解(合理即可)
。③转移时将氯化钠溶液转移到
细口瓶
细口瓶
瓶中,贴上标签备用。(5)约取3mL5%的碳酸氢钠溶液于试管中,向其中滴入5滴收集的溶液,发现溶液中出现白色沉淀,同时又有持续的气泡产生,向得到的浊液中继续加入过量稀盐酸,溶液逐渐变澄清,同时产生气体,两次产生的气体通入澄清石灰水中,均能使澄清石灰水变浑浊,该实验中碳酸氢钠溶液和氯化钙溶液反应的化学方程式为
CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O
CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O
。探究四:“氯化钙除湿剂”中主要含量的测定
(6)经过进一步测定,“氯化钙除湿剂”的主要成分是CaCl2•nH2O,其在一定温度下发生反应:CaCl2•nH2O
一定温度
2
2
。(写出计算过程,n取整数)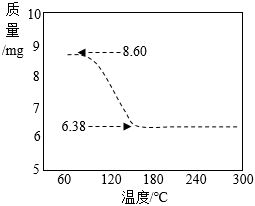
【答案】砖红;硝酸银;CaCl2+2AgNO3=Ca(NO3)2+2AgCl↓;放出;取少量氯化钙固体放入试管中,向试管中加入适量的水,用手触摸试管外壁,感觉温度升高,所以氯化钙溶解是放出热量的;酸度计或pH计;称量;搅拌,加速溶解(合理即可);细口瓶;CaCl2+2NaHCO3=CaCO3↓+2NaCl+CO2↑+H2O;2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/24 8:0:9组卷:78引用:2难度:0.4
相似题
-
1.钠的焰色反应颜色呈( )
发布:2024/11/8 8:0:1组卷:21引用:1难度:0.6 -
2.今年的洞头海岛烟花节上,小科欣赏到了一种黄色烟花,他很好奇烟花的黄色是怎么来的?在查阅资料得知,原来黄色烟花中有加入硝酸钠(NaNO3)。
(1)小科提出了两个假设:
假设1:硝酸钠中的钠离子在灼烧时使烟火呈现出黄色。
假设2:。
(2)小科查阅了以下资料:
资料一:多种金属或它们的化合物在灼烧时使火焰呈现特殊的颜色,这在化学上叫焰色反应。
资料二:硝酸铜[Cu(NO3)2]、硝酸钾(KNO3)中含有硝酸根离子,氯化钠(NaCl)、硫酸钠 (Na2SO4)中均含有铜离子。
他在实验室内走了一圈,找到了装有硝酸铜,硝酸钾,氧化钠、硫酸钠的试剂瓶,接下来他的操作。发现火焰不是黄色,于是他得出结论:。发布:2024/8/4 8:0:9组卷:1引用:0难度:0.6 -
3.焰色反应火焰呈黄色的是( )
发布:2024/5/27 14:0:0组卷:14引用:1难度:0.6


