中国古代已掌握了铜冶炼和铸造技术,现代铜冶炼废气、废水需经过处理后排放。
Ⅰ.铜的冶炼与防腐
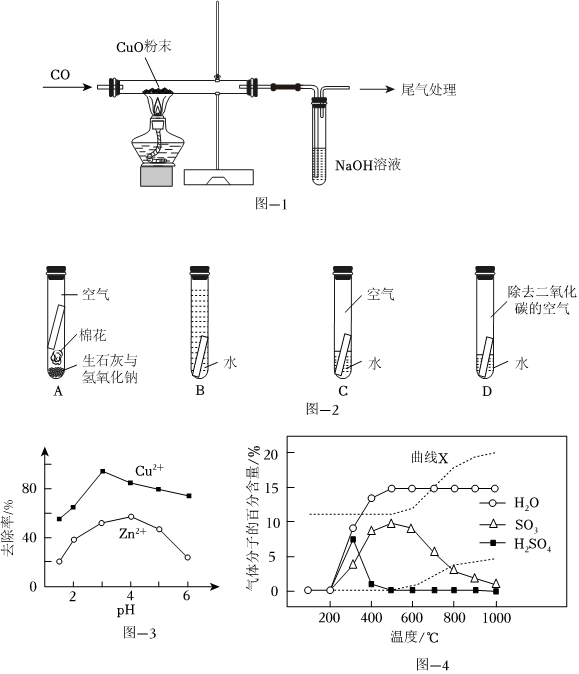
(1)如图-1所示一氧化碳还原氧化铜的实验,硬质玻璃管内出现 黑色固体逐渐变红黑色固体逐渐变红(现象),证明反应已经发生。
(2)上述实验获得的Cu中含有少量黑色的CuO。请补充完整提纯铜的实验方案:将所得固体置于烧杯中,加入足量稀硫酸充分反应至黑色固体完全溶解,过滤,蒸馏水洗涤滤渣2-3次加入足量稀硫酸充分反应至黑色固体完全溶解,过滤,蒸馏水洗涤滤渣2-3次,干燥。(可选用的试剂:稀H2SO4、AgNO3溶液、NaOH溶液,蒸馏水)
(3)《周礼•考工记》中记载了铸造各类青铜器的配方。铜和青铜的相关性质见下表,推断铜冶炼过程中熔入锡的作用有 降低铜的熔点,提高铜的硬度降低铜的熔点,提高铜的硬度。
| 铜 | 青铜(含25%的锡) | |
| 熔点 | 1085℃ | 800℃ |
| 硬度 | 3.0 | 5~6.6 |
(4)某同学设计实验探究铜锈蚀产生铜绿[Cu2(OH)2CO3]的条件(如图-2所示),图中铜片上最不易产生铜绿的是
A
A
(填序号)。Ⅱ.湿法炼铜废水的处理
(5)湿法炼铜产生酸性废水,含有的CuSO4、ZnSO4可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对Cu2+、Zn2+去除率的影响如图-3所示。
①pH<3时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
。②相同pH条件下,Cu2+的去除率远高于Zn2+的原因可能是
Fe能置换出Cu,但不能置换出Zn
Fe能置换出Cu,但不能置换出Zn
。Ⅲ.工业铜冶炼废气的处理
(6)工业上利用反应 Cu2S+O2
高温
经过水洗除尘后,烟气中部分气体分子的百分含量(
气体中某分子的数目
气体分子总数
①图中虚线表示SO2或O2的变化,其中曲线X表示的物质是
SO2
SO2
。②当500℃烟气温度下降时,SO3含量降低的主要原因是
SO3+H2O=H2SO4
SO3+H2O=H2SO4
(用化学方程式表示)。③温度低于200℃时,烟气中几乎不存在水分子的主要原因是
温度较低时,烟气产生液态硫酸有吸水性
温度较低时,烟气产生液态硫酸有吸水性
。【答案】黑色固体逐渐变红;加入足量稀硫酸充分反应至黑色固体完全溶解,过滤,蒸馏水洗涤滤渣2-3次;降低铜的熔点,提高铜的硬度;A;Fe+H2SO4=FeSO4+H2↑;Fe能置换出Cu,但不能置换出Zn;SO2;SO3+H2O=H2SO4;温度较低时,烟气产生液态硫酸有吸水性
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/11 8:0:9组卷:976引用:2难度:0.5
相似题
-
1.下列实验现象描述正确的是( )
发布:2024/10/7 0:0:1组卷:63引用:4难度:0.6 -
2.用如图装置进行一氧化碳还原氧化铜的实验,请回答:

(1)装置C中玻璃管内产生的现象是.
(2)实验开始时的操作顺序是(填序号).
①先点燃酒精灯,后通入一氧化碳 ②先通入一氧化碳,后点燃酒精灯
(3)试比较实验过程中,装置B和D中出现的现象分别为、.
(4)装置E在该实验中的作用是.发布:2024/8/26 9:0:8组卷:181引用:3难度:0.5 -
3.下列装置是一种改进的用一氧化碳还原氧化铜的实验装置。

(1)若先对氧化铜进行加热,再通一氧化碳,可能产生的后果是。
(2)写出装置A中发生反应的化学方程式:
(3)根据B装置中出现的现象,可以判断反应是否开始,则装置B中的试剂是,发生反应的化学方程式为。
(4)装置C的作用是。
(5)C装置的收集方法叫,收集到C瓶中的气体应如何处理。发布:2024/8/15 5:0:1组卷:10引用:2难度:0.3
相关试卷


