元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。
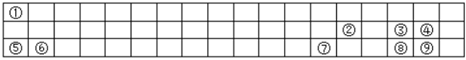
Ⅰ.如图是元素周期表的一部分,回答下列问题:
(1)⑧所对应的元素在周期表中的位置 第三周期第ⅥA族第三周期第ⅥA族。
(2)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质的电子式 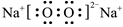
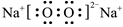 。
。
(3)写出⑤的最高价氧化物对应的水化物与⑦的最高价氧化物反应的化学方程式 Al2O3+2NaOH=2NaAlO2+H2OAl2O3+2NaOH=2NaAlO2+H2O。
(4)比较④与⑨的简单气态氢化物的稳定性 HFHF>HClHCl(填化学式)。
Ⅱ.某小组为探究Cl2、Br2、I2的氧化性强弱,设计实验如图:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
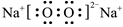
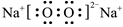
| 序号 | 实验① | 实验② |
| 实验操作 |
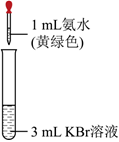
|

|
| 现象 | 溶液变为黄色 |
溶液变蓝 溶液变蓝
|
2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
。(6)实验②观察到的现象是
溶液变蓝
溶液变蓝
,甲同学根据此现象得出结论:氧化性Br2>I2。乙同学认为实验②不能充分证明氧化性Br2>I2,其理由是 实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质
实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质
。【答案】第三周期第ⅥA族;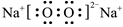 ;Al2O3+2NaOH=2NaAlO2+H2O;HF;HCl;溶液变蓝;2Br-+Cl2=2Cl-+Br2;溶液变蓝;实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质
;Al2O3+2NaOH=2NaAlO2+H2O;HF;HCl;溶液变蓝;2Br-+Cl2=2Cl-+Br2;溶液变蓝;实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质
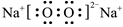 ;Al2O3+2NaOH=2NaAlO2+H2O;HF;HCl;溶液变蓝;2Br-+Cl2=2Cl-+Br2;溶液变蓝;实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质
;Al2O3+2NaOH=2NaAlO2+H2O;HF;HCl;溶液变蓝;2Br-+Cl2=2Cl-+Br2;溶液变蓝;实验①反应后的黄色溶液里可能存在未反应完的Cl2,Cl2也能使碘离子氧化成碘单质【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/25 8:0:9组卷:20引用:2难度:0.6


