大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是 改变反应速率改变反应速率。
(2)某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快,对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
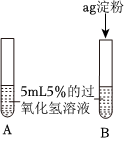 |
A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①B中产生的气体是 氧气 氧气 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | B中又产生大量使带火星木条复燃的气体;滤渣质量为ag | ②淀粉的 质量和化学性质 质量和化学性质 在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
【实验拓展】
该小组设计了如图1所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据见表:
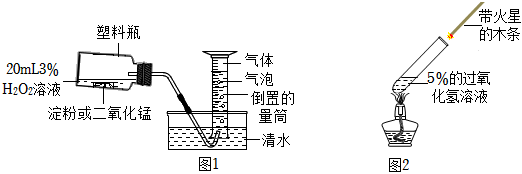
| 实验编号 | 3%过氧化氢溶液的体积 | 其他物质质量 | 待测数据 |
| Ⅰ | 20mL | 淀粉0.5g | a |
| Ⅱ | 20mL | 二氧化锰0.5g | b |
生成25mL气体需要的时间
生成25mL气体需要的时间
;若a>b,则可得出的结论是 二氧化锰催化效果比淀粉好
二氧化锰催化效果比淀粉好
。(4)写出二氧化锰催化过氧化氢分解的文字(或符号)表达式
过氧化氢水+氧气或H2O2H2O+O2
二氧化锰
M
n
O
2
过氧化氢水+氧气或H2O2H2O+O2
。二氧化锰
M
n
O
2
(5)温度升高过氧化氢的分解速率会加快,某同学取足量5%的过氧化氢溶液进行加热,如图2所示,可实验中带火星的木条往往难以复燃,请解释原因
氧气中混有较多的水蒸气
氧气中混有较多的水蒸气
。【考点】判断某物质在化学反应中是否做催化剂.
【答案】改变反应速率;氧气;质量和化学性质;生成25mL气体需要的时间;二氧化锰催化效果比淀粉好;过氧化氢水+氧气或H2O2H2O+O2;氧气中混有较多的水蒸气
二氧化锰
M
n
O
2
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/7 7:0:2组卷:29引用:3难度:0.5
相似题
-
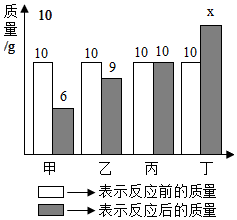 1.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )发布:2024/8/9 8:0:9组卷:54引用:4难度:0.7
1.甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )发布:2024/8/9 8:0:9组卷:54引用:4难度:0.7 -
2.在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:
下列说法中,不正确的是( )物质 甲 乙 丙 丁 反应前质量/g 18 1 2 32 反应后质量/g X 26 2 12 发布:2024/8/31 3:0:11组卷:45引用:4难度:0.4 -
3.一定条件下,甲、乙、丙、丁、戊五种物质在密闭容器中发生反应,反应一段时间后,测得反应前后各种物质的质量(单位:g)如图所示,下列说法不正确的是( )
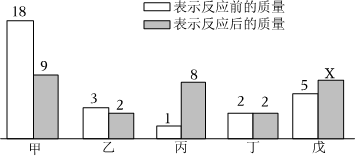 发布:2024/8/3 8:0:9组卷:12引用:1难度:0.5
发布:2024/8/3 8:0:9组卷:12引用:1难度:0.5


