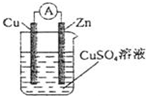
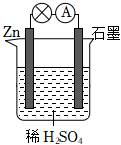
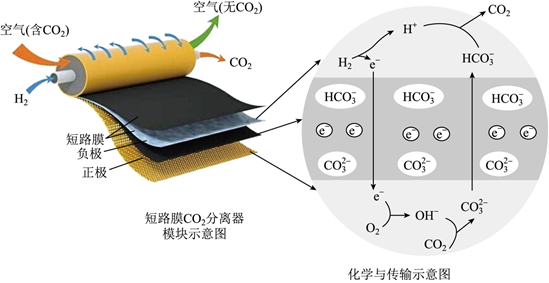
含N元素的部分物质对环境有影响。含NO、NO2的废气会引起空气污染,含NO-2、NO-3、NH+4的废水会引起水体富营养化,都需要经过处理后才能排放。消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1)利用电化学装置可消除氮氧化物污染,变废为宝。
①化学家正在研究尿素动力燃料电池直接去除城市废水中的尿素,既能产生净化的水,又能发电,尿素燃料电池结构如图所示:
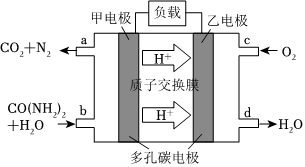
甲的电极反应式为 CO(NH2)2-6e-+H2O=CO2↑+N2↑+6H+CO(NH2)2-6e-+H2O=CO2↑+N2↑+6H+;理论上每净化1mol尿素,消耗O2的体积约为 33.633.6L(标准状况下)。
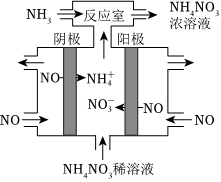
②图为电解NO制备NH4NO3的装置。该装置中阴极的电极反应式为 NO+5e-+6H+=NH+4+H2ONO+5e-+6H+=NH+4+H2O;“反应室”中发生反应的离子方程式为 NH3+H+=NH+4NH3+H+=NH+4。
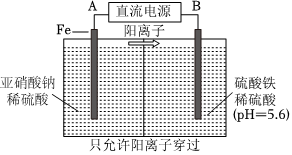
(2)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图所示,写出电解时铁电极的电极反应式 Fe-2e-=Fe2+Fe-2e-=Fe2+。随后,铁电极附近有无色气体产生,可能原因是 生成的亚铁离子将溶液中的NO-2还原成N2生成的亚铁离子将溶液中的NO-2还原成N2。
(3)工业上以钛基氧化物涂层材料为阳极,碳纳米管修饰的石墨为阴极,电解硝酸钠和硫酸钠混合溶液,可使NO-3转变为NH+4,后续再将NH+4反应除去。②其他条件不变,只向混合溶液中投入一定量NaCl,后续去除NH+4的效果明显提高,溶液中氮元素含量显著降低。可能原因是 Cl-在阳极上失去电子生成Cl2,氯气具有强氧化性,可将NH+4氧化成N2,使溶液中氮元素的含量明显降低Cl-在阳极上失去电子生成Cl2,氯气具有强氧化性,可将NH+4氧化成N2,使溶液中氮元素的含量明显降低。
NO
-
2
NO
-
3
NH
+
4
N
H
+
4
N
H
+
4
N
H
+
4
N
H
+
4
N
O
-
2
N
O
-
2
NO
-
3
NH
+
4
NH
+
4
NH
+
4
N
H
+
4
N
H
+
4
【答案】CO(NH2)2-6e-+H2O=CO2↑+N2↑+6H+;33.6;NO+5e-+6H+=+H2O;NH3+H+=;Fe-2e-=Fe2+;生成的亚铁离子将溶液中的还原成N2;Cl-在阳极上失去电子生成Cl2,氯气具有强氧化性,可将氧化成N2,使溶液中氮元素的含量明显降低
N
H
+
4
N
H
+
4
N
O
-
2
N
H
+
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/11 14:0:2组卷:120引用:3难度:0.5