当前位置:
试题详情
查阅一款新型清洁产品“爆炸盐”的说明书,发现其主要有效成分为过碳酸钠。为测定爆炸盐中过碳酸钠(2Na2CO3•3H2O2)的质量分数,采用如图甲的测定实验:取样品10克溶于热水,待溶液不再产生气泡,分别测量整个装置在反应前、后的总质量,整理数据如表:

| 待测的量 | 反应前总质量 | 反应后总质量 |
| 电子天平示数(克) | 213.66 | 212.70 |
2Na2CO3•3H2O2═2Na2CO3+3H2O2,2H2O2
△
(1)上述过程中产生的氧气,需要分解多少克的过氧化氢(H2O2)才能得到?
(2)若图甲实验中不使用干燥装置,直接让容器敞口完成上述测量实验,将导致过碳酸钠质量分数的测量值
偏大
偏大
。(3)“爆炸盐”去污源于H2O2分解产生活性氧,若产氧过快会使易掉色的衣物出现褪色,图乙为小组同学在老师的指导下,测出图甲中产氧速度随时间变化及反应产热导致温度变化的关系图,结合图乙,提出一项措施来减少“爆炸盐”对衣物的褪色作用,并从图乙中寻找证据来支持你所提出的措施的合理性:
水量一定时,减少爆炸盐的用量,12-14分钟温度在升高,但随着反应物浓度降低,产生氧气的速度减小
水量一定时,减少爆炸盐的用量,12-14分钟温度在升高,但随着反应物浓度降低,产生氧气的速度减小
。【考点】根据化学反应方程式的计算.
【答案】偏大;水量一定时,减少爆炸盐的用量,12-14分钟温度在升高,但随着反应物浓度降低,产生氧气的速度减小
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/19 8:0:9组卷:18引用:0难度:0.5
相似题
-
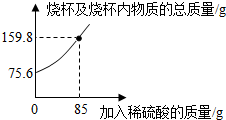 1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为g.
(2)计算样品中铁的质量分数(写出解题过程).发布:2025/1/9 8:0:2组卷:139引用:39难度:0.1 -
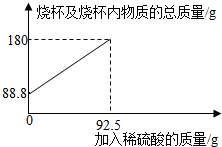 2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了10g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:4引用:1难度:0.3 -
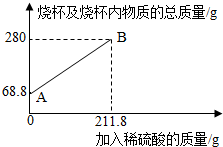 3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)求样品中铁的质量分数;反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了20g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:8引用:1难度:0.3


