1810年,英国化学家戴维以大量事实为依据,确认一种黄绿色气体是一种新元素组成的单质——氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。

(1)仪器b的名称为 分液漏斗分液漏斗。某同学认为该实验装置存在一处明显的不足,其改进措施为 在装置F后接一个尾气处理装置在装置F后接一个尾气处理装置。
(2)仪器a中发生反应的化学方程式为 MnO2+4HCl(浓) △ MnCl2+Cl2↑+2H2OMnO2+4HCl(浓) △ MnCl2+Cl2↑+2H2O。根据氯气的性质D中的收集装置可以选择 ③③(填序号)。

(3)下列有关该实验的说法中不正确的是 ACAC(填字母)。
A.将b中溶液换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.F中红色布条褪色,证明氯气具有漂白性
D.可用湿润的淀粉碘化钾试纸检验氯气是否收集满
(4)实验室还可用等物质的量的Cl2与Na2CO3的水溶液反应制取Cl2O,同时生成NaHCO3和NaCl,反应的化学方程式为 2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl。
△
△
【答案】分液漏斗;在装置F后接一个尾气处理装置;MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;③;AC;2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/17 3:0:2组卷:20引用:1难度:0.6
相似题
-
1.为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如图.其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸.干燥红色布条、浓硫酸、湿润红色布条.
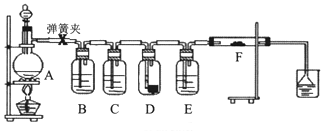
请回答:
(1)E中浓硫酸的作用.
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是.
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有.
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量.发布:2025/1/15 8:0:2组卷:17引用:1难度:0.3 -
2.如图是某同学设计的氯气制备及性质验证实验装置。相关说法正确的是( )
 发布:2025/1/15 8:0:2组卷:20引用:2难度:0.8
发布:2025/1/15 8:0:2组卷:20引用:2难度:0.8 -
3.实验室中模拟用甲烷与氯气反应得到的副产品来制取盐酸,原理如图,下列说法不正确的是( )
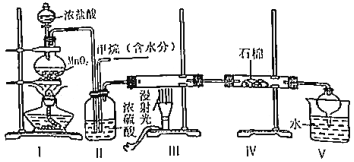 发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7
发布:2024/12/30 17:0:5组卷:61引用:1难度:0.7


