在生产生活中,金属锰及其化合物用途广泛。
(一)对金属锰及其化合物的认识
(1)植物生长需要微量的锰,这里的锰是指 BB(选填序号)。
A.原子
B.元素
C.单质
(2)地铁列车的钢轨材料是高锰钢(主要成分铁、锰、碳),高锰钢属于 混合物混合物(选填“纯净物”或“混合物”)。车身作喷漆处理既美观又防锈,其防锈原理是 隔绝水和氧气隔绝水和氧气。
(3)华为手机使用的是锂电池,锂电池质量轻、容量大,其反应原理是锂与二氧化锰反应生成亚锰酸锂(LiMnO2),该反应的化学方程式是 Li+MnO2=LiMnO2Li+MnO2=LiMnO2。
(4)菱锰矿(主要成分是MnCO3,含少量FeCO3),向一定量矿石中加入稀盐酸,观察到有大量气泡产生,且反应前后金属元素的化合价保持不变,推断反应后溶液中含有的金属阳离子主要是 Mn2+、Fe2+Mn2+、Fe2+(填离子符号)。
(二)碳酸锰的制备
MnCO3是一种高性能磁性材料。以软锰矿(主要成分为MnO2)为原料制备MnCO3的主要流程如下。已知:MnCO3难溶于水,在100℃时开始分解。
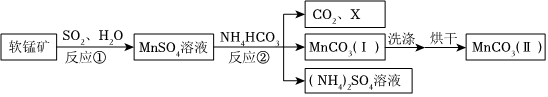
(5)原料软锰矿在使用之前通常需粉碎,其目的是 增大接触面积,使反应更充分,反应速率更快增大接触面积,使反应更充分,反应速率更快。
(6)已知X是一种常见的无色液体,则反应②的化学方程式为 MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+CO2↑+H2OMnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+CO2↑+H2O。
(7)反应②中加入NH4HCO3溶液时,往往需要控制温度在30~35℃,温度不宜过高的原因是 NH4HCO3 △ NH3↑+CO2↑+H2ONH4HCO3 △ NH3↑+CO2↑+H2O(用化学方程式表示)。
(8)产品MnCO3(Ⅱ)比MnCO3(Ⅰ)更纯净,原因是产品MnCO3(Ⅰ)经过洗涤、烘干后,表面附着的水及 (NH4)2SO4(NH4)2SO4等杂质已被除去。
(9)为了获得纯净的MnCO3,烘干时需要控制的条件是 小于100℃小于100℃。
(三)碳酸锰热分解产物的研究
MnCO3及锰的氧化物加热分解的温度如下。
MnCO3300℃
MnO2600℃
MnaOb900℃
MnO
称取4.60gMnCO3样品置于装置A中,进行热分解实验。控制不同的温度对样品加热,测得剩余固体质量随温度的变化如图2所示。
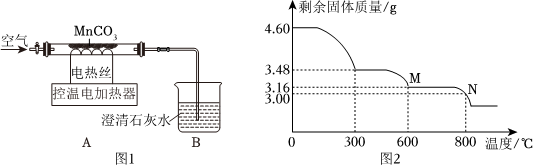
(10)通入空气,焙烧MnCO3到300℃时,观察到装置B中澄清石灰水变浑浊,写出装置A中反应的化学方程式为 2MnCO3+O2 △ 2MnO2+2CO22MnCO3+O2 △ 2MnO2+2CO2。
(11)加热至300-900℃时,锰的氧化物分解会分解产生一种常见气体,该气体为 氧气氧气。
(12)当加热到800℃时,N点固体的成分是 Mn2O3和MnOMn2O3和MnO,对应物质的质量比为 79:7179:71。
△
△
300 ℃ |
600 ℃ |
900 ℃ |
△
△
【答案】B;混合物;隔绝水和氧气;Li+MnO2=LiMnO2;Mn2+、Fe2+;增大接触面积,使反应更充分,反应速率更快;MnSO4+2NH4HCO3=(NH4)2SO4+MnCO3↓+CO2↑+H2O;NH4HCO3 NH3↑+CO2↑+H2O;(NH4)2SO4;小于100℃;2MnCO3+O2 2MnO2+2CO2;氧气;Mn2O3和MnO;79:71
△
△
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/24 2:0:8组卷:141引用:2难度:0.4
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
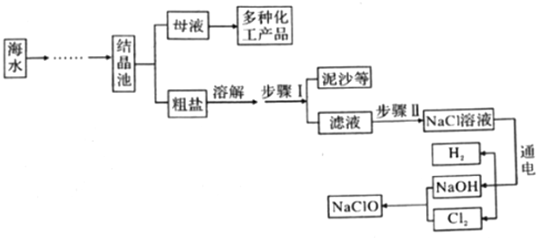
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
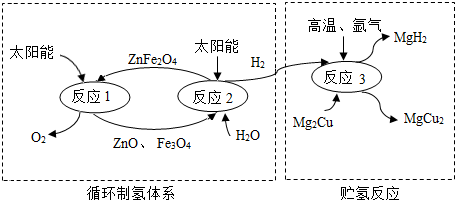 2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5 -
3.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7


