氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得。
(1)工业上利用氮气和氢气在一定条件下反应制氨气,反应的化学方程式为 N2+3H2 一定条件 2NH3N2+3H2 一定条件 2NH3。
(2)小华为探究氨气溶于水是否发生化学反应,设计并完成下表实验:
一定条件
一定条件
| 实验操作 | 实验现象 | 结论 |
| 将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 | 干燥的氨气不能使酚酞变色 |
| 将 浸有酚酞溶液的湿润滤纸 浸有酚酞溶液的湿润滤纸 ,放入盛有干燥氨气的集气瓶中 |
试纸变红 试纸变红
|
氨气能与水反应 |
氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅
氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅
。(4)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化。她取200mL1%的稀盐酸,测定其pH为1.3,煮沸并蒸发一段时间后,测定其pH为0.9,则稀盐酸经加热煮沸后浓度
增大
增大
(填“增大”、“减小”或“不变”)。为进一步研究,取稀盐酸平均分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗盐酸的量:①大于
大于
②(填“大于”、“小于”或“等于”)。(5)为除去氯化钠溶液中的碳酸钠,小林设计了如图方案:
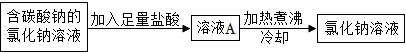
你认为上述方案
不合理
不合理
(填“合理”或“不合理”),原因是 加热无法除去溶液中过量的HCl
加热无法除去溶液中过量的HCl
。(6)小李欲测定氢氧化钠溶液变质情况,取出100g该溶液,向其中逐滴滴加溶质质量分数为14.6%的稀盐酸,加入稀盐酸的质量与生成气体的质量之间的关系如图所示。据此推测并计算:
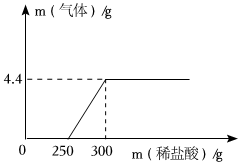
①该氢氧化钠溶液的变质情况:
部分变质
部分变质
。(选填“完全变质”或“部分变质”)②该氢氧化钠溶液中碳酸钠的质量为
10.6
10.6
g。③当加入300g稀盐酸充分反应后,计算所得溶液中溶质的质量分数。(结果精确到0.1%,写出计算过程)
【答案】N2+3H2 2NH3;浸有酚酞溶液的湿润滤纸;试纸变红;氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅;增大;大于;不合理;加热无法除去溶液中过量的HCl;部分变质;10.6
一定条件
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/14 8:0:9组卷:21引用:2难度:0.5
相似题
-
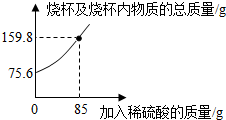 1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
1.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为52.2g的烧杯中,然后缓慢加入一定质量的稀硫酸,当加稀硫酸质量为85g时,反应恰好完全(杂质不反应且产生的气体全部逸出),反应过程中的质量关系如图.完成下列问题:
(1)该实验取用的样品质量为g.
(2)计算样品中铁的质量分数(写出解题过程).发布:2025/1/9 8:0:2组卷:139引用:39难度:0.1 -
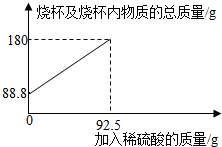 2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
2.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入92.5g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了10g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:4引用:1难度:0.3 -
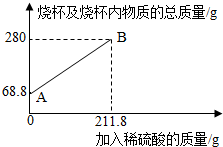 3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
3.为测定某碳素钢样品中铁的质量分数,现取一定质量的样品粉末于质量为51.8克的烧杯中,然后逐步加入一定质量分数的稀硫酸,当加入211.8g稀硫酸时恰好完全反应,加入稀硫酸的质量与烧杯及烧杯内物质的总质量的关系如图。
(1)该实验取用的样品质量为g。
(2)求样品中铁的质量分数;反应后所得溶液中的溶质的质量分数。(写出计算过程,结果保留一位小数)
(3)反应结束后,小明不慎向烧杯中多加了20g稀硫酸,若在图中补绘此过程中稀硫酸的质量与烧杯及烧杯内物质的总质量的关系图,所得线段的终点位于线段AB延长线的(填:上方、下方或线上)。发布:2025/1/9 8:0:2组卷:8引用:1难度:0.3


