某试液中只可能含有K+、NH+4、Fe2+、Cl-、SO2-4、CO2-3中的若干种离子。某同学进行了如下实验:
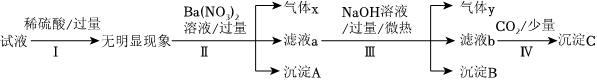
请仔细阅读下列已知条件:
①NH+4+OH- △ NH3↑+H2O;
②Fe2++H++NO-3→Fe3++NO↑+H2O(未配平);
③不考虑与水的反应及水电离出的H+和OH-。
回答下列问题:
(1)由实验Ⅰ可知,试液中一定不存在的离子为 CO2-3CO2-3(填离子符号),判断的理由为 CO2-3+2H+═CO2↑+H2OCO2-3+2H+═CO2↑+H2O(用离子方程式表示)。
(2)由实验Ⅱ可知:
①原试液中一定存在的离子为 Fe2+Fe2+(填离子符号)。
②滤液a的颜色可能为 黄色黄色。
③气体x为 NONO(填化学式)。
(3)沉淀B为 Fe(OH)3Fe(OH)3(填化学式)。
(4)生成沉淀C的离子方程式为 CO2+Ba2++2OH-=BaCO3↓+H2OCO2+Ba2++2OH-=BaCO3↓+H2O。
NH
+
4
SO
2
-
4
CO
2
-
3
NH
+
4
△
NO
-
3
CO
2
-
3
CO
2
-
3
CO
2
-
3
CO
2
-
3
【考点】常见离子的检验方法.
【答案】;+2H+═CO2↑+H2O;Fe2+;黄色;NO;Fe(OH)3;CO2+Ba2++2OH-=BaCO3↓+H2O
CO
2
-
3
CO
2
-
3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/10/23 0:0:2组卷:22引用:1难度:0.7
相似题
-
1.某无色溶液,其中可能存在Na+、Ba2+、
、S2-、AlO-2、SO2-3.取该溶液进行有关实验,实验结果如图所示.SO2-4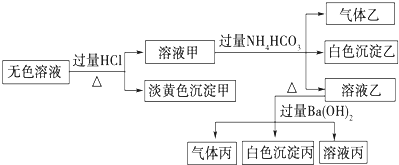
回答下列问题:
(1)沉淀甲的化学式为.
(2)由溶液甲生成沉淀乙的离子方程式为.
(3)沉淀丙中一定含有(填化学式,下同),可能含有.
(4)综合上述信息,该溶液中肯定存在的离子有.
(5)该溶液显性(填酸性、碱性或中性),若要检验其酸碱性,下图操作正确的是.
请用离子方程式表示显碱性的原因:.发布:2024/12/30 6:0:2组卷:10引用:2难度:0.3 -
2.在实验室鉴定氯酸钾晶体和1-氯丙烷中的氯元素,现设计了下列实验操作程序:①滴加AgNO3溶液;②加入NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取残渣;⑦用HNO3酸化。(填序号)
(1)鉴定氯酸钾中氯元素的操作步骤依次是
(2)鉴定1-氯丙烷中氯元素的操作步骤依次是。发布:2024/12/30 8:0:15组卷:67引用:8难度:0.5 -
3.为检验某种阳离子为Na-的溶液中含有的阴离子是SO42-、CO32-、OH-还是Cl-,下列设计的方案合理的是( )
发布:2024/12/30 6:30:2组卷:9引用:2难度:0.6


