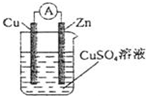
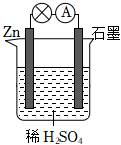
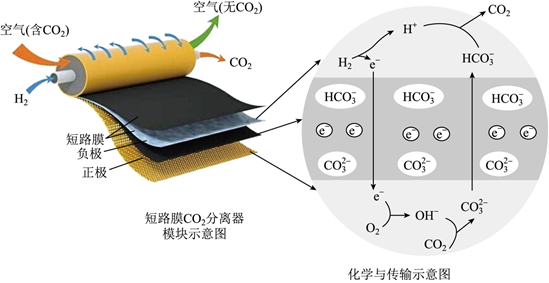
电池广泛应用于日常生活、生产和科学技术等方面。
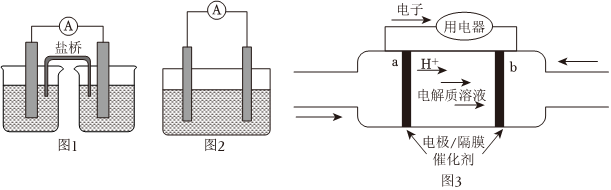
(1)化学兴趣小组同学根据所学知识,利用氧化还原反应Zn+Cu2+═Cu+Zn2+设计成如图所示的两种原电池,图1装置与图2装置相比优点是 避免氧化剂和还原剂直接接触,能量转化效率更高避免氧化剂和还原剂直接接触,能量转化效率更高,当反应进行到一段时间后取出电极材料,测得某一电极减少了6.5g,则该原电池反应共转移的电子数目是 0.2NA0.2NA。
(2)铅蓄电池在放电时发生的电池反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O。正极反应为 PbO2+2e-+4H++SO2-4═PbSO4+2H2OPbO2+2e-+4H++SO2-4═PbSO4+2H2O。若电解液硫酸的体积为2L(反应过程溶液体积变化忽略不计),放电过程中外电路中转移3mol电子,则硫酸浓度由5mol/L下降到 3.53.5mol/L。
(3)“2023中国(上海)国际氢能与燃料电池技术展览会”将于2023年7月26-28日在上海国家会展中心举办,展会以“绿色赋能氢启未来”为主题。通过促进氢能与燃料电池技术领域的国际交流,为人类社会的可持续发展做出贡献,某种氢氧燃料电池的内部结构如图3所示:
①右侧b电极的电极反应为:O2+4e-+4H+=2H2OO2+4e-+4H+=2H2O。
②当有0.1mol电子通过导线时,左侧消耗标准状况下气体的体积是 1.12L1.12L。
(4)根据甲醇在酸性电解质溶液中与氧气生成二氧化碳和水的反应,设计一种燃料电池。该电池工作时,负极上发生的反应为 CH3OH-6e-+H2O=CO2+6H+CH3OH-6e-+H2O=CO2+6H+。理论上消耗1mol甲醇,该电池能放出电量 5.78×1055.78×105(保留3位有效数字)C。(一个电子的电量q=1.60×10-19C,NA=6.02×1023mol-1)
SO
2
-
4
SO
2
-
4
【考点】原电池与电解池的综合.
【答案】避免氧化剂和还原剂直接接触,能量转化效率更高;0.2NA;PbO2+2e-+4H++═PbSO4+2H2O;3.5;O2+4e-+4H+=2H2O;1.12L;CH3OH-6e-+H2O=CO2+6H+;5.78×105
SO
2
-
4
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/19 8:0:9组卷:23引用:1难度:0.6