小金查阅资料发现:氢气还原氧化铜的实验中,若反应过程通入氢气时间不够,得到的固体产物是铜和氧化亚铜组成的混合物。于是他对反应产物的生成情况进行了如下探究:利用图甲所示实验装置,称取若干份质量均为0.6克的氧化铜,在相同条件下分别用氢气还原不同时间并检测固体中氧化亚铜的质量,结果如图乙。

(1)利用图甲装置进行氢气还原氧化铜的实验时,正确实验操作顺序为 ③①②④③①②④。
①加热
②停止加热
③通入制好的纯净氢气
④停止通氢气
(2)为解释实验结果,小金对氢气还原氧化铜的反应过程提出如下假设:反应经历2CuO+H2 △ Cu2O+H2O、H2+Cu2O △ 2Cu+H2O两个反应,且在同一条件下两个反应同时进行而不是分步进行。若分步进行,则生成的Cu2O的最大质量为 0.540.54克。再根据图乙所示的探究结果分析,同时进行的依据是 如果分步进行,氧化亚铜最大质量应该是0.54g,而不是0.3218g如果分步进行,氧化亚铜最大质量应该是0.54g,而不是0.3218g。
(3)为确保反应所得固体中氧化亚铜尽可能少,可采取的措施是 加热条件下通入氢气的时间足够长加热条件下通入氢气的时间足够长。
△
△
【考点】碳、一氧化碳、氢气还原氧化铜实验.
【答案】③①②④;0.54;如果分步进行,氧化亚铜最大质量应该是0.54g,而不是0.3218g;加热条件下通入氢气的时间足够长
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/19 8:0:9组卷:177引用:1难度:0.5
相似题
-
1.用如图所示装置进行实验,回答下列问题。

(1)装置Ⅰ的实验目的是。能否用硫磺代替本实验中的红磷?。
(2)Ⅱ中电解反应的化学方程式为;该实验得到的直接结论是。
(3)完成图Ⅲ所示实验时,应先(选填“通 CO”或“点燃酒精喷灯”),试管中发生反应的化学方程式为,尾部的酒精灯处发生的反应属于什么基本反应类型?。同学们在实验前后均进行了准确称量,发现实验后玻璃管及其内容物的质量减小了0.8g,则他们理论上可以得到g铜。发布:2024/12/17 4:30:2组卷:35引用:1难度:0.5 -
2.用甲乙丙三套装置进行H2、C、CO还原CuO的实验并检验产物(已知白色粉末无水硫酸铜遇水变蓝色)、分析上述三个实验,下列说法错误的是( )
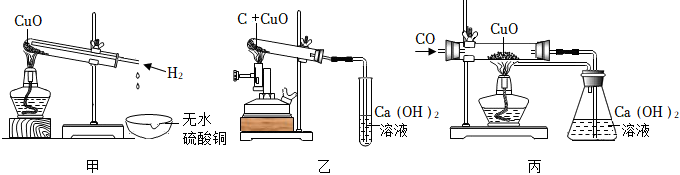 发布:2024/12/28 12:30:2组卷:71引用:2难度:0.5
发布:2024/12/28 12:30:2组卷:71引用:2难度:0.5 -
3.某气体可能由H2、CO、CO2、H2O、HCl中的一种或几种组成,为确定其成分,进行如下实验:

气体通过有关装置时观察到的现象如下:
试推断:装置编号 A B C D E 试剂 硝酸银溶液 澄清石灰水 氧化铜粉末 澄清石灰水 无水硫酸铜 现象 无明显变化 变浑浊 变红色 无明显变化 变蓝色
(1)装置A的作用是。
(2)根据上表中的现象判断该气体中一定含有。
(3)若想证明该气体的确切成分、应如何改进装置?写出具体改进方案。发布:2024/12/28 15:30:1组卷:120引用:2难度:0.5


