某实验小组的同学们为研究稀盐酸与氢氧化钠能否发生化学反应,设计如下的实验方案。

【方案一】测定溶液pH的变化证明二者发生化学反应。图1为用pH传感器测定两溶液混合时pH的变化曲线。
(1)该实验过程是先在烧杯中加入 氢氧化钠/NaOH氢氧化钠/NaOH溶液,再向烧杯中滴加另一种溶液。
(2)同学们测定了不同时刻溶液的pH,结果如下:A.10;B.9;C.7;D.3,以上测定结果中,能说明二者已经发生了化学反应的数值 CDCD(填序号)。
(3)b点所表示的溶液中,所含溶质为 NaClNaCl(填化学式)。
(4)验证反应后c点溶液中稀盐酸有剩余,请选出一种盐类物质并写出发生的化学方程式 Na2CO3+2HCl=2NaCl+H2O+CO2↑(合理即可)Na2CO3+2HCl=2NaCl+H2O+CO2↑(合理即可)。
【方案二】利用化学反应中的能量变化证明氢氧化钠与盐酸发生化学反应。
【查阅资料】中和反应放热。
【进行实验】
(5)在不使用温度计的情况下,通过如图2所示的装置进行实验,观察到红墨水 向右移动向右移动(填“向左移动”、“向右移动”或“不动”),证明二者发生反应(不考虑滴加的盐酸液体引起的体积变化)。
【反思交流】
(6)有的同学提出,该现象不足以证明盐酸和氢氧化钠固体发生了化学反应,理由是 NaOH固体溶解也放热NaOH固体溶解也放热。
【方案三】利用图3实验证明二者发生化学反应。
(7)步骤Ⅰ没有明显的实验现象,为证明反应发生,步骤Ⅱ可选用下列药品中的 BDBD。
A.AgNO3溶液
B.酚酞溶液
C.Na2CO3溶液
D.FeCl3溶液
E.CO2
【考点】中和反应及其应用;溶液的酸碱性与pH的关系.
【答案】氢氧化钠/NaOH;CD;NaCl;Na2CO3+2HCl=2NaCl+H2O+CO2↑(合理即可);向右移动;NaOH固体溶解也放热;BD
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/7 8:0:9组卷:233引用:2难度:0.3
相似题
-
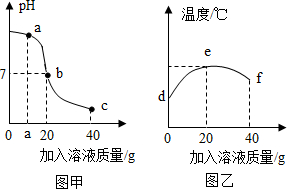 1.某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图甲所示,溶液的温度变化如图乙所示(不考虑反应过程中热量损失)。下列说法错误的是( )发布:2024/12/25 17:0:2组卷:71引用:3难度:0.6
1.某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像如图甲所示,溶液的温度变化如图乙所示(不考虑反应过程中热量损失)。下列说法错误的是( )发布:2024/12/25 17:0:2组卷:71引用:3难度:0.6 -
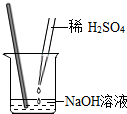 2.小明同学用如图所示的方法做酸碱中和实验,采用酚酞试液作指示剂,恰好完全中和时溶液的颜色为( )发布:2024/12/25 17:0:2组卷:68引用:3难度:0.9
2.小明同学用如图所示的方法做酸碱中和实验,采用酚酞试液作指示剂,恰好完全中和时溶液的颜色为( )发布:2024/12/25 17:0:2组卷:68引用:3难度:0.9 -
3.某研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实验.下列选项正确的是( )
选项 所用试剂 现象和结论 A 硫酸铜溶液 出现蓝色沉淀,则氢氧化钠过量 B 氯化钡溶液 出现白色沉淀,则硫酸过量 C 铜丝 有气泡产生,则硫酸过量 D 无色酚酞溶液 溶液不变色,则恰好完全反应 发布:2024/12/25 17:30:2组卷:46引用:2难度:0.7


