中国古代化学科技是中华文明瑰宝。
(1)《天工开物》记载“点铅勾锡”是炼锡的关键一步,即加铅能使锡较易熔化流出,原因是合金的熔点比组成它的纯金属的 低低(选填“高”或“低”)。
(2)《淮南万毕术》中记载“曾青得铁则化为铜”,先用孔雀石制取硫酸铜,再用“湿法炼铜”获得铜。其流程如图:
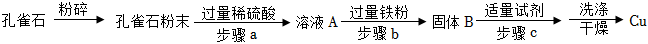
①孔雀石需要粉碎,这样做的目的是 增大反应物之间的接触面积,使反应更快更充分增大反应物之间的接触面积,使反应更快更充分。
②步骤a的反应方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑。加入的稀硫酸需过量的目的是 使孔雀石中的Cu2(OH)2CO3完全反应使孔雀石中的Cu2(OH)2CO3完全反应。
③溶液A中的阳离子是 Cu2+、H+Cu2+、H+(写离子符号),固体B的成分是 Fe、CuFe、Cu(写化学式)。
(3)“卓筒井”是手工制盐的活化石。其工艺流程有:钻井→汲卤→晒卤→滤卤→煎盐。
①“汲卤”获得的卤水中氯化钠的质量分数为7%—10%(20℃时氯化钠的溶解度为36.0g),则该卤水是氯化钠的 不饱和不饱和(填“饱和”或“不饱和”)溶液。
②“晒卤”过程中溶液的溶质质量分数 变大变大(填“变大”、“变小”或“不变”)。
③“滤卤”与实验室过滤的原理一样,都是为了除去液体中的 不溶性不溶性(填“不溶性”或“可溶性”)杂质。
④“煎盐”与实验室 蒸发蒸发操作相似,当 大部分固体析出大部分固体析出时停止加热,利用余热使水分蒸干。所得精盐中含有氯化钙、氯化镁和硫酸钠,向其中加水溶解后依次加入稍过量的氯化钡、氢氧化钠和碳酸钠溶液,充分反应后过滤,所得滤液中含有的杂质是 NaOH、Na2CO3NaOH、Na2CO3(写化学式)。
【答案】低;增大反应物之间的接触面积,使反应更快更充分;使孔雀石中的Cu2(OH)2CO3完全反应;Cu2+、H+;Fe、Cu;不饱和;变大;不溶性;蒸发;大部分固体析出;NaOH、Na2CO3
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/12 8:0:9组卷:26引用:2难度:0.5
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
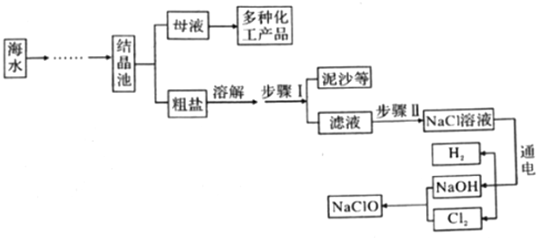
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
2.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7 -
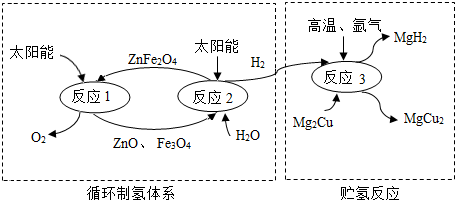 3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5


