浩瀚的海洋中蕴藏着丰富的资源,可从海水中提取食盐、制取镁、溴等化工产品。回答下列问题:
Ⅰ.粗盐精制
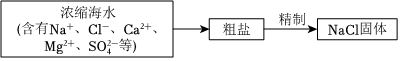
除去粗盐中的Ca2+、Mg2+、SO2-4等杂质离子时,粗盐溶解后加入沉淀剂:①过量的Na2CO3溶液;②过量的BaCl2溶液;③过量的NaOH溶液。过滤除去沉淀,再加入适量的盐酸。
(1)加入沉淀剂的正确顺序的是 bcbc(填字母标号)。
a.①②③
b.②①③
c.③②①
(2)加入适量盐酸,反应的离子方程式有 2H++CO2-3═H2O+CO2↑2H++CO2-3═H2O+CO2↑和 H++OH-═H2OH++OH-═H2O。
Ⅱ.海水提镁

(3)“沉镁”过程中加入的试剂是 石灰乳石灰乳。由无水MgCl2获得Mg的化学方程式是 MgCl2(熔融) 通电 Mg+Cl2↑MgCl2(熔融) 通电 Mg+Cl2↑。
Ⅲ.海水提溴
主要工业生产流程如图所示:
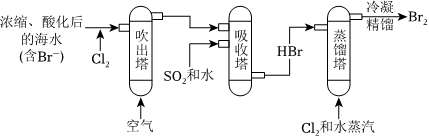
(4)向“吹出塔”中鼓入空气的目的是将 Br2Br2(填化学式)吹出。
(5)“吸收塔”中发生反应的化学方程式为 SO2+Br2+2H2O=2HBr+H2SO4SO2+Br2+2H2O=2HBr+H2SO4。
(6)“蒸馏塔”溶液中溴的浓度比“吹出塔”溶液中溴的浓度 高高(填“高”“低”或“相等”)。
S
O
2
-
4
CO
2
-
3
CO
2
-
3
通电
通电
【答案】bc;2H++═H2O+CO2↑;H++OH-═H2O;石灰乳;MgCl2(熔融) Mg+Cl2↑;Br2;SO2+Br2+2H2O=2HBr+H2SO4;高
CO
2
-
3
通电
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/7/21 8:0:9组卷:23引用:1难度:0.7
相似题
-
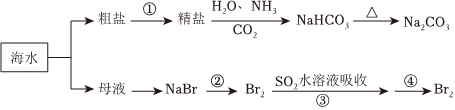
1.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是( )
 发布:2024/12/30 3:30:1组卷:130引用:9难度:0.6
发布:2024/12/30 3:30:1组卷:130引用:9难度:0.6 -
2.海水是化学元素的宝库,从海水中可以提取或生产多种化工原料,如食盐、氯气、单质溴、镁、纯碱等,它们在工农业生产中有着广泛的用途.根据学过的知识回答下列问题:
(1)某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液.
①其反应原理为:(用离子方程式表示).
②配制250mL 4.0mol•L-1NaOH溶液,需要用到的玻璃仪器,除烧杯、玻璃棒外,还必须用到的是.
(2)工业制得粗硅后,再与氯气等物质发生反应,最终得到纯硅.请写出工业制取粗硅的化学方程式:
(3)金属镁被誉为“国防金属”,若镁起火,不能用CO2来灭火,其原因可用化学方程式表示为
(4)①若Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法是,
②若NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的方法是.发布:2024/10/27 17:0:2组卷:11引用:1难度:0.5 -
3.海水资源开发利用的部分过程如图所示:
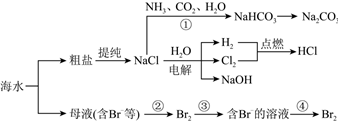
下列说法正确的是( )发布:2024/11/3 6:0:1组卷:51引用:3难度:0.7


