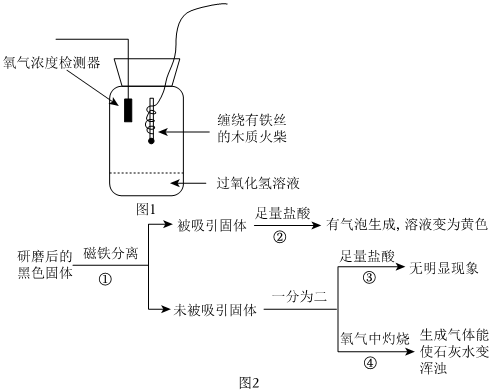
实验小组同学对铁丝燃烧实验进行深入研究。实验装置见图1。在检测器检测的氧气浓度升高且稳定后,伸入缠绕不同形状铁丝并点燃的木质火柴,记录实验数据。
Ⅰ.探究铁丝燃烧时间的影响因素
【进行实验】
观察到铁丝燃烧可分为两个阶段:
剧烈燃烧阶段现象:剧烈燃烧,火星四射,放热,生成黑色固体剧烈燃烧,火星四射,放热,生成黑色固体。
缓慢燃烧阶段现象:铁丝先变红,后变暗,瓶底出现黑色固体。
| 铁丝螺旋形状 | 小螺旋 | 大螺旋 | ||||
| 组号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 氧气浓度 | 67% | 80% | 84% | 74% | 80% | 87% |
| 剧烈燃烧时间/s | 13’15 | 9’19 | 7’08 | 11’03 | 9’19 | 7’07 |
| 缓慢燃烧时间/s | 2’14 | 2’06 | 1’04 | 1’06 | 2’06 | 1’04 |
(1)实验开始时,向过氧化氢溶液中加入
二氧化锰
二氧化锰
,可以使氧气浓度快速升高。(2)铁丝剧烈燃烧的现象为
剧烈燃烧,火星四射,放热,生成黑色固体
剧烈燃烧,火星四射,放热,生成黑色固体
。(3)设计①②③组实验的目的是
比较氧气浓度不同时,剧烈燃烧时间和缓慢燃烧时间的长短
比较氧气浓度不同时,剧烈燃烧时间和缓慢燃烧时间的长短
。(4)实验证明铁丝燃烧时间与铁丝螺旋形状无关,与氧气浓度有关。其中能证明燃烧时间与铁丝螺旋形状无关的证据是
②⑤中剧烈燃烧时间和缓慢燃烧时间相等
②⑤中剧烈燃烧时间和缓慢燃烧时间相等
。Ⅱ.探究生成黑色固体成分
【查阅资料】
ⅰ.Fe3O4+8HCl═2FeCl3+FeCl2+4H2O
ⅱ.铁和Fe3O4均可以被磁铁吸引,Fe2O3和木炭不会被磁铁吸引。
ⅲ.木质火柴柄主要成分为纤维素,纤维素含有碳、氢、氧三种元素。
【提出猜想】
黑色固体中含有Fe3O4,可能含有下列成分:①Fe、②Fe2O3、③木炭
【进行实验】如图2所示。
【解释与结论】
(5)猜想黑色固体中含有木炭的依据是
④中生成能使澄清石灰水变浑浊的气体
④中生成能使澄清石灰水变浑浊的气体
。(6)用化学方程式解释被吸引固体加入稀盐酸产生气泡的原因
Fe+2HCl═FeCl2+H2↑
Fe+2HCl═FeCl2+H2↑
。(7)操作④的目的是
证明固体中含有木炭
证明固体中含有木炭
。(8)有关黑色固体成分的结论为
黑色固体含有四氧化三铁、铁、木炭
黑色固体含有四氧化三铁、铁、木炭
。【考点】实验探究物质的组成成分以及含量.
【答案】剧烈燃烧,火星四射,放热,生成黑色固体;二氧化锰;剧烈燃烧,火星四射,放热,生成黑色固体;比较氧气浓度不同时,剧烈燃烧时间和缓慢燃烧时间的长短;②⑤中剧烈燃烧时间和缓慢燃烧时间相等;④中生成能使澄清石灰水变浑浊的气体;Fe+2HCl═FeCl2+H2↑;证明固体中含有木炭;黑色固体含有四氧化三铁、铁、木炭
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/24 8:0:9组卷:59引用:1难度:0.5
相似题
-
 1.家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.
1.家庭厨房就是一个充盈的化学小世界,“柴米油盐酱醋糖”中包含着许多化学内容.
(1)米、面的主要成分都是由三种元素组成的淀粉,淀粉属于糖类.
(2)水瓶内的水垢主要成分是碳酸钙,可用(填一种调味品)除去.
(3)白糖与红糖主要成分都是蔗糖.利用活性炭的性,可将红糖脱色成白糖.
(4)市场上销售的香肠、盐水鸭、榨菜、豆腐干等食品,常采用真空包装,其目的是防止食品而变质.
(5)味精是烹制菜肴时常用的调味品,小明研究某品牌味精包装上的部分文字说明后,想测定此味精中氯化钠的含量.
[查阅资料]NaCl+AgNO3=AgCl↓+NaNO3,谷氨酸钠的存在不影响NaCl性质.
[实验过程]
①称取该味精样品10.0g,并溶于蒸馏水
②加入过量的硝酸银溶液,过滤
③用蒸馏水反复洗涤沉淀多次
④将沉淀烘干、称量,测得固体质量为5.74g
根据上述实验步骤回答下列有关问题:
①过滤操作所需要的仪器除烧杯、铁架台(带铁圈)、玻璃棒外,还需要的玻璃仪器是.
②试通过计算确定此样品中NaCl质量分数与其包装上标注的含量是否相符.发布:2025/1/6 8:0:1组卷:68引用:2难度:0.5 -
2.化学兴趣小组同学们在老师的指导下对市售某品牌“钙片”的补钙原理、成分以及功效展开了项目化学习的探究。
【查阅资料】
(1)该补钙剂的主要成分有碳酸钙、维生素D3、硫酸锌、水果香料等。
(2)维生素D3、水果香料都不溶于水也不与酸反应,维生素D3主要作用是促进人体对钙的吸收。
项目一:探究“钙片”补钙原理。
【分析交流】
“钙片”中钙以碳酸钙形式存在,“钙片”进入胃首先要通过人体胃酸对其进行溶解后方可被吸收。
【进行实验】
【反思评价】服用“钙片”时,采用实验方案 实验现象 实验结论或化学方程式 取适量“钙片”粉末于试管中,滴加足量 。化学方程式 (填“吞服”或“嚼服”)的服药方式更有利促进胃肠吸收。
项目二:探究“钙片”中是否含有硫酸锌。
项目三:探究“钙片”的功效。实验方案 实验现象 实验结论 另取少量“钙片”粉末于试管中,加足量水,充分溶解,取适量上层清液于试管中,加入几滴 。“钙片”中含有硫酸锌。
【交流讨论】
该补钙剂适用于中老年人治疗因缺钙导致的患者。老师建议大家应注意平时的饮食补钙,牛奶、鱼类等食物除富含营养素外,是较好的补钙食物,应该多食用。发布:2025/1/3 16:0:5组卷:30引用:1难度:0.5 -
 3.酸、碱、盐种类繁多,与人类生活和生产关系密切。请回答下列问题:
3.酸、碱、盐种类繁多,与人类生活和生产关系密切。请回答下列问题:
(1)造纸业会产生大量含NaOH的碱性废水,需经处理至中性排放。
①写出NaOH的俗称:(一个即可)。
②若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸9.8t(H2SO4的质量分数为10%)。可以处理的废水质量为t。
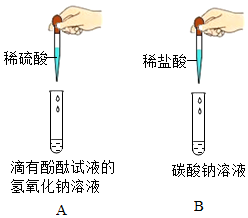
(2)某化学兴趣小组做了如图所示的两个实验。完成A、B两个实验后,同学们将实验后的废液倾倒入一个废液缸中,发现废液呈红色,小组同学对废液成分展开了如下探究。(该题实验过程中所用溶液浓度较低;氯化钙溶液和氯化钡溶液显中性;实验中如涉及硫酸钙、氢氧化钙等微溶物,均可看做可溶物)
【交流讨论】小组同学经讨论分析后一致认为废液中一定含有的溶质有氯化钠和(酚酞除外)。
【提出猜想】废液中还含有的物质:
猜想一:NaOH;
猜想二:Na2CO3;
猜想三:(填化学式)。
【实验验证】
甲同学取少量废液于试管中,向其中加入过量的氯化钙溶液,通过观察现象,得出了正确结论。若猜想二正确,甲同学观察到的现象:有白色沉淀生成,;请写出发生反应的化学方程式:。
【交流与反思】乙同学认为,将甲同学实验中的氯化钙溶液换成氯化钡溶液,也能得出正确结论。你认为乙同学的观点是否正确并说明你的理由:。发布:2025/1/3 8:0:1组卷:93引用:1难度:0.5


