CH4 既是一种重要的能源,也是一种重要的化工原料。
(1)甲烷的电子式为
 。
。
(2)甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要通入适量空气使部分甲烷燃烧,其目的是提供CH4分解所需的能量提供CH4分解所需的能量。
(3)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理图1所示,则通入a气体的电极名称为负极负极,通入 b气体的电极反应式O2+4H++4e-=2H2OO2+4H++4e-=2H2O。(质子交换膜只允许H+通过)
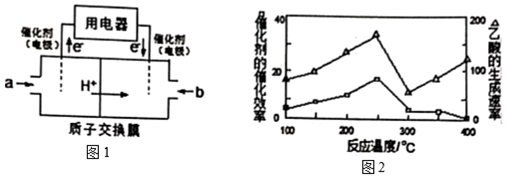
(4)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图2所示,则该反应的最佳温度应控制在250℃250℃左右。
②CH4与CO2可直接转化成乙酸的原子利用率为100%100%。
(5)碳正离子(例如:CH3+、CH5+、(CH3)3C+等)是有机反应中间体,CH5+碳正离子是由CH4在“超强酸”中获得一个H+而得到,而CH5+失去H2可得CH3+.(CH3)3C+去掉H+后生成电中性有机分子,该分子的结构简式为(CH3)2C=CH2(CH3)2C=CH2。
(6)CH4与Cl2在光照条件下可发生反应。
①实验室中用如图3所示的装置进行实验。
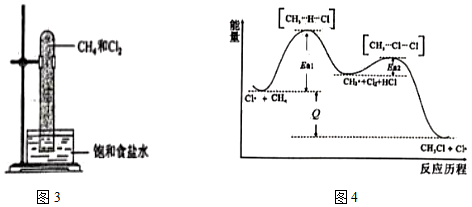
在光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是DD。
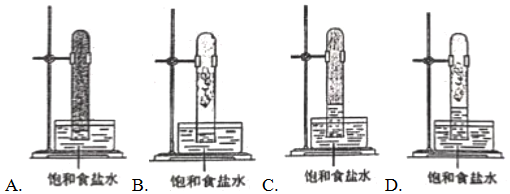
②CH4与Cl2生成CH3Cl的反应过程,中间态物质的能量关系见图4.有关说法不正确的是BB。(填序号)
A.Cl•是由Cl2 在光照下化学键断裂生成的,该过程可表示为: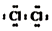 光
光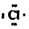
B.反应过程一定无CH3CH3生成
C.图示过程放出热量
D.CH4 转化为CH3Cl,C-H键发生了断裂


光
【答案】 ;提供CH4分解所需的能量;负极;O2+4H++4e-=2H2O;250℃;100%;(CH3)2C=CH2;D;B
;提供CH4分解所需的能量;负极;O2+4H++4e-=2H2O;250℃;100%;(CH3)2C=CH2;D;B
 ;提供CH4分解所需的能量;负极;O2+4H++4e-=2H2O;250℃;100%;(CH3)2C=CH2;D;B
;提供CH4分解所需的能量;负极;O2+4H++4e-=2H2O;250℃;100%;(CH3)2C=CH2;D;B【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/10 0:21:48组卷:196引用:3难度:0.5


