某化学兴趣小组的同学依据所学金属的化学性质展开探究活动。
(1)资料显示,铜锌合金外观和黄金相似,为区分黄金制品和铜锌合金制品,化学兴趣小组同学依据所学金属的化学性质设计实验,就可以区分出铜锌合金,他们的实验步骤和现象是:将黄金制品和铜锌合金分别 灼烧,变黑的是铜锌合金,没有变化的是黄金制品灼烧,变黑的是铜锌合金,没有变化的是黄金制品。
(2)铜、铁、铝是生活中常见的金属,某化学兴趣小组的同学利用粗细相同、新打磨的铝丝、铁丝和铜丝,展开探究活动。小组同学依据所学金属的化学性质
活动一:探究金属的活动性:如图1所示,取长短相同的三种金属加入酸中。现象和结论记录如下:
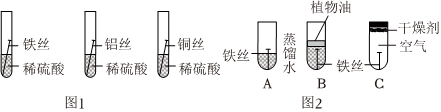
| 金属 | 实验现象 | 实验结论 |
| 铝丝 | 铝丝表面有大量气泡产生且反应剧烈 | 活动性: Al>Fe>Cu Al>Fe>Cu |
| 铁丝 | 铁丝表面有少量气泡产生且反应缓慢 | |
| 铜丝 | 无现象 |
①实验过程中铁丝与稀硫酸反应的化学反应方程式是
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
。②探究这三种金属的活动性,还可选用的试剂组合是(至少三种)
铝丝、硫酸亚铁溶液、铜丝;或硫酸铝溶液、铁丝、硫酸铜溶液;或铝丝、氯化亚铁溶液、铜丝;或氯化铝溶液、铁丝、氯化铜溶液(合理即可)
铝丝、硫酸亚铁溶液、铜丝;或硫酸铝溶液、铁丝、硫酸铜溶液;或铝丝、氯化亚铁溶液、铜丝;或氯化铝溶液、铁丝、氯化铜溶液(合理即可)
(不用酸溶液)。活动二:探究铁生锈的条件
如图2,三支试管内铁丝最先生锈的是
A
A
(填序号),A与B对比说明铁丝生锈需要 与氧气接触
与氧气接触
。在焊接铁制品前常用稀盐酸清除其表面的锈,该反应的化学方程式是 Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
。【能力发展】保护金属资源的有效途径
防止金属制品腐蚀;或合理开采金属资源;或回收利用废旧金属;或寻找金属代用品等(答案合理即可)
防止金属制品腐蚀;或合理开采金属资源;或回收利用废旧金属;或寻找金属代用品等(答案合理即可)
(写一条)。【答案】灼烧,变黑的是铜锌合金,没有变化的是黄金制品;Al>Fe>Cu;Fe+H2SO4=FeSO4+H2↑;铝丝、硫酸亚铁溶液、铜丝;或硫酸铝溶液、铁丝、硫酸铜溶液;或铝丝、氯化亚铁溶液、铜丝;或氯化铝溶液、铁丝、氯化铜溶液(合理即可);A;与氧气接触;Fe2O3+6HCl=2FeCl3+3H2O;防止金属制品腐蚀;或合理开采金属资源;或回收利用废旧金属;或寻找金属代用品等(答案合理即可)
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/15 8:0:8组卷:19引用:1难度:0.5
相似题
-
1.根据图示设计的实验来进一步认识金属的化学性质和金属的活动性顺序。
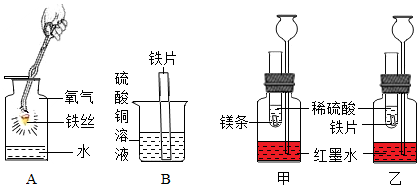
(1)写出实验A中反应的化学方程式:。
(2)实验B中可观察到铁片的表面出现,说明铁的金属活动性比铜(填“强”或“弱”)。
(3)若想探究镁、铁、铜三种金属的活动性强弱,小清同学提出在实验B的基础上增加实验甲和乙,便可得出结论。试管内的镁片和铁片表面均被打磨洁净,且形状、大小相同;同时加入等质量和等浓度的稀硫酸。
①乙装置中发生反应的化学方程式为。
②观察到试管中有气泡产生且长颈漏斗中甲的液面上升比乙(填“快”或“慢”)时,可以证明镁的金属活动性比铁的强。
③若甲、乙实验所用的金属均过量,则甲装置中产生的H2质量(填“大于”“小于”或“等于”)乙装置中产生的H2质量。
④小亮同学指出若想探究这三种金属的活动性强弱,只需使用三种药品即可达到实验目的,请你帮助小亮完成其实验方案。操作 现象 结论 将镁片和铜片分别放入氯化亚铁溶液中 放入铜片的氯化亚铁溶液中 ,放入镁片的氯化亚铁溶液的颜色由金属的活动性强弱关系为Mg>Fe>Cu 发布:2024/12/7 8:0:1组卷:77引用:1难度:0.5 -
2.2019年版第五套人民币5角硬币的材质已由“钢芯镀铜合金”改为“钢芯镀镍”,其表面色泽也因此由
色变为银白色。化学兴趣小组决定,探究制造5角硬币的三种主要金属(铁、铜、镍)活动性顺序。
【查阅资料】
(1)硫酸镍溶液显绿色,Ni的化合价通常为+2价。
(2)镍能与稀硫酸反应,生成硫酸镍和氢气。
【提出猜想】猜想①:;猜想②:Fe>Ni>Cu。
【实验探究】
(1)甲组同学将一块表面洁净的镍片放入稀硫酸中,观察到的实验现象是,有关反应的化学方程式是。
(2)乙组同学将一块表面洁净的镍片浸入硫酸亚铁溶液中,一会儿取出,发现镍片表面无明显变化,说明猜想(填“①”或“②”)成立。
(3)丙组同学用铜片、硫酸镍溶液和进行实验,也得出了三种金属的活动性顺序。
【拓展延伸】
(1)某电镀公司的检修员利用工作之便,将镍网放入含有金盐的电镀液中偷偷“吸取”黄金,该盗窃手法利用了(填反应的基本类型)原理。该员工窃取贵重物品的行为,必将受到法律的制裁。
(2)金属活动性实际上是金属在水溶液中失去电子的能力大小。下列事实可以判断M、N两种金属活动性顺序的是(填序号)。
①M能和盐酸反应而N不能
②M、N分别放入盐酸中比较反应剧烈程度
③常温下M能与氧气反应而N不能
④M能从N的盐溶液中置换出N发布:2024/12/25 14:0:2组卷:229引用:5难度:0.5 -
3.化学小组为探究铁、铜、锌、银的金属活动性顺序,设计如下三个实验(其中金属均已打磨,其形状、大小及同种稀盐酸的用量均相同):
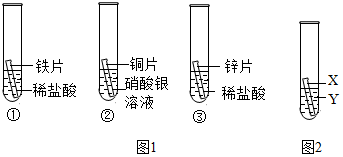
(1)实验①的化学方程式为;一段时间后,观察到实验②的铜片表面有银白色固体附着,这说明铜比银的活动性(填“强”或“弱”)。
(2)甲同学认为通过实验①和③可比较锌和铁的金属活动性,他依据的实验现象是。
(3)乙、丙两位同学认为上述实验方案不足以得出四种金属的活动顺序,并在上述实验的基础上,利用金属
不同的化学性质分别补充了一个实验(图2所示),都实现了探究的目的。乙同学的实验:X是金属,Y是溶液;丙同学的实验:X是金属,Y是溶液。发布:2024/12/25 17:30:2组卷:46引用:4难度:0.5
相关试卷


