高纯碳酸锂(Li2CO3)是制造电动汽车电池的原料之一。
(1)电池中存在LiMnO2,已知锂元素显+1价,则锰元素的化合价为 +3+3;锂电池充电时是将电能转化为 BB(填字母)。
A.机械能
B.化学能
C.热能
(2)粗碳酸锂(含有Na+、K+、Ca2+等杂质离子),制备高纯碳酸锂的工艺流程如图:
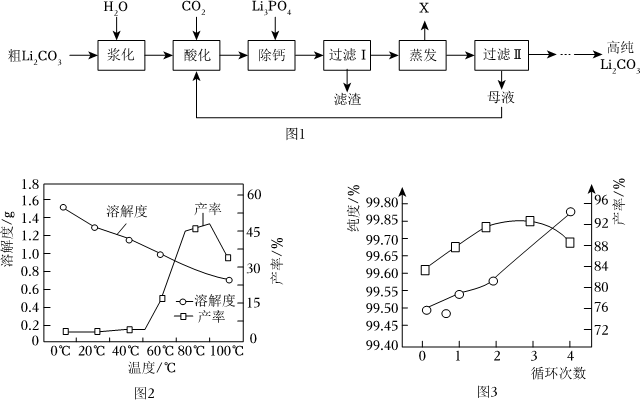
查阅资料:碳酸锂能与水、二氧化碳反应生成碳酸氢锂(LiHCO3),碳酸氢锂易溶于水,加热会分解为碳酸锂。
①浆料“酸化”时主要反应的化学方程式为 Li2CO3+CO2+H2O=2LiHCO3Li2CO3+CO2+H2O=2LiHCO3。“酸化”时温度不宜过高的原因可能是 温度过高,碳酸氢锂加热会分解为碳酸锂温度过高,碳酸氢锂加热会分解为碳酸锂,判断酸化过程已经结束的明显现象为 浆料变得澄清浆料变得澄清。
②已知在不同温度下“蒸发”时碳酸锂的产率与溶解度关系如图2,据图可知,90℃以下随着反应温度升高,碳酸锂产率明显增加,其原因可能是 碳酸锂的溶解度随着温度升高而减小碳酸锂的溶解度随着温度升高而减小。
③母液循环次数对纯度、产率的影响如图3所示,据图可知,循环不宜超过 33次,其原因是 循环次数增多,溶液中的钠离子,钾离子会溶解的更多,浓度增大从而降低产品的纯度循环次数增多,溶液中的钠离子,钾离子会溶解的更多,浓度增大从而降低产品的纯度。
④为了获得较多高纯Li2CO3,过滤Ⅱ后应选用 热水热水(填“热水”或“冷水”)洗涤沉淀2~3次。
【考点】物质的相互转化和制备;有关元素化合价的计算.
【答案】+3;B;Li2CO3+CO2+H2O=2LiHCO3;温度过高,碳酸氢锂加热会分解为碳酸锂;浆料变得澄清;碳酸锂的溶解度随着温度升高而减小;3;循环次数增多,溶液中的钠离子,钾离子会溶解的更多,浓度增大从而降低产品的纯度;热水
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/6/17 8:0:9组卷:96引用:2难度:0.5
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
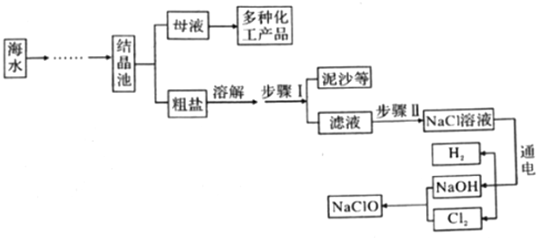
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
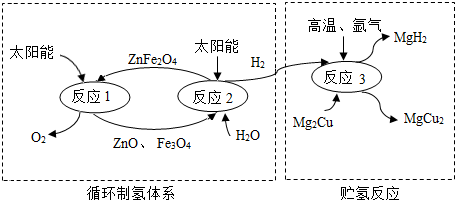 2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
2.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5 -
3.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7


