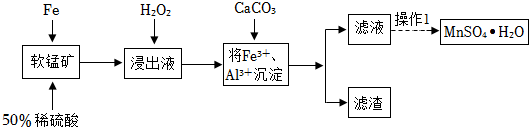
软锰矿主要成分为MnO2,并含有少量Fe2O3、Al2O3、MgO、SiO2等杂质,工业上制备硫酸锰晶体(MnSO4⋅H2O)的流程如图所示:
【资料查阅】
软锰矿中MnO2发生的反应:MnO2+2Fe+4H2SO4=MnSO4+Fe2(SO4)3+2H2O。
(1)在软锰矿的杂质中属于非金属氧化物的物质是 SiO2SiO2(填化学式)。
(2)加入稀硫酸时,氧化铝发生的反应是 Al2O3+3H2SO4=Al2(SO4)3+3H2OAl2O3+3H2SO4=Al2(SO4)3+3H2O(用化学方程式表示)。
(3)加入碳酸钙后溶液的pH逐渐增大,可将浸出液中杂质离子Fe3+、Al3+形成氢氧化物除去,根据下表“有关氧氧化物沉淀pH”,则应控制溶液的pH范围为 5.0~8.3之间5.0~8.3之间。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 1.8 | 4.1 | 8.3 | 9.4 |
| 完全沉淀pH | 3.2 | 5.0 | 9.8 | 12.4 |
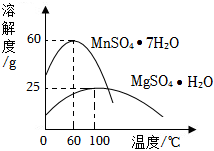
操作1是指在
100
100
(填“60”或“100”)℃时,蒸发水分、浓缩结晶,得到较多的MnSO4•H2O,然后 趁热过滤
趁热过滤
(填操作),洗涤、干燥。(5)此项工艺需配制稀硫酸mg,则需取用98%的浓硫酸的质量为
0.51m
0.51m
g(计算结果保留两位有效数字)。【答案】SiO2;Al2O3+3H2SO4=Al2(SO4)3+3H2O;5.0~8.3之间;100;趁热过滤;0.51m
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/5/12 8:0:9组卷:38引用:2难度:0.5
相似题
-
1.新冠肺炎疫情防控期间,西安市各学校开展全域喷洒低浓度、有效成分是次氯酸钠的“84”消毒液进行消毒。如图所示是模拟制备“84”消毒液的流程(Cl2是一种黄绿色的有毒气体)。请回答下列问题:
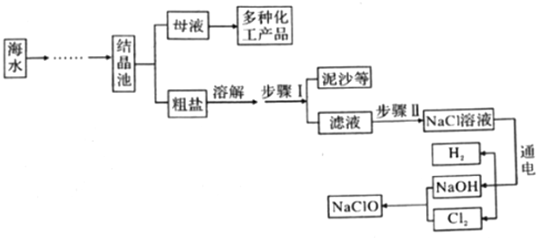
(1)NaOH的俗称为(写一种)。
(2)步骤Ⅱ中,通常用碳酸钠溶液除去滤液中的氯化钙杂质,请写出有关反应的化学方程式。
(3)电解水时,一般在水中加入少量NaOH以增强水的导电性,不能加入NaCl的原因是。发布:2025/1/3 8:0:1组卷:6引用:1难度:0.5 -
2.某种家用的消毒液的主要成分是次氯酸钠(NaClO),制取NaClO的化学方程式为:Cl2+2NaOH=NaClO+NaCl+H2O,下列说法错误的是( )
发布:2025/1/3 8:0:1组卷:71引用:1难度:0.7 -
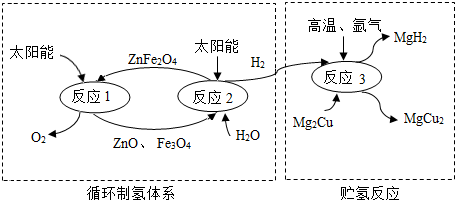 3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5
3.如图是制取与贮存氢气的一种方法,Mg2Cu是一种贮氢合金,吸氢后生成MgH2和MgCu2合金的混合物(M),MgH2+2HCl═MgCl2+2H2↑,下列说法不正确的是( )发布:2024/12/31 8:0:1组卷:48引用:2难度:0.5


