钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
Ⅰ.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 BB(填字母);
A.铁铲 B.铁锅 C.刀具
(2)“纳米a-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 氧气和水氧气和水;
Ⅱ.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从其氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式:3CO+Fe2O3 高温 2Fe+3CO23CO+Fe2O3 高温 2Fe+3CO2;
(2)高炉炼铁中,焦炭的作用除了可以提供热量外,还能 反应生成还原剂一氧化碳反应生成还原剂一氧化碳;
Ⅲ.实验探究炼铁原理:
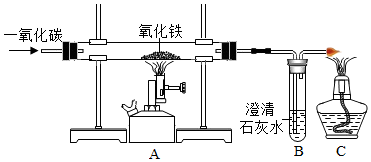
某化学兴趣小组的同学利用如图装置模拟工业炼铁的过程,请按要求填空:
(1)实验时装置A中的现象是 红棕色粉末逐渐变成黑色红棕色粉末逐渐变成黑色;
(2)B中发生反应的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2OCO2+Ca(OH)2=CaCO3↓+H2O;
(3)实验过程中,CO的作用有 ①②③④①②③④(填序号);
①CO气体作为反应物;②实验开始时,排尽装置中的空气,防止加热时发生爆炸;③停止加热后,防止A中生成物被氧化;④停止加热后防止B中的溶液倒吸入A中。
Ⅳ.拓展延伸
利用上面的装置测定某铁的氧化物中铁元素和氧元素的质量比。实验记录数据如下:①装铁的氧化物的硬质玻璃管的质量为20g;②硬质玻璃管与铁的氧化物的质量共为26.4g;③通入一氧化碳并加热至铁的氧化物全部转化为铁后,生成的二氧化碳全部被澄清石灰水吸收,且B中生成沉淀的质量为12g。
根据以上实验记录,计算此铁的氧化物中铁元素和氧元素的质量比 7:37:3。
高温
高温
【答案】B;氧气和水;3CO+Fe2O3 2Fe+3CO2;反应生成还原剂一氧化碳;红棕色粉末逐渐变成黑色;CO2+Ca(OH)2=CaCO3↓+H2O;①②③④;7:3
高温
【解答】
【点评】
声明:本试题解析著作权属菁优网所有,未经书面同意,不得复制发布。
发布:2024/8/11 2:0:1组卷:78引用:2难度:0.6
相似题
-
1.某化学兴趣小组用以下装置探究炼铁的原理.
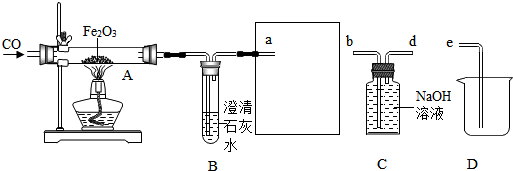
(1)加热Fe2O3之前要先通一会儿CO,目的是.
(2)方框中连接的是C和D,导管接口的连接顺序为a→()→()→(),如果导管连接错误,后果是.
(3)玻璃管A中发生反应的化学方程式为,用这种方法“炼”得的铁与工业上炼出的生铁在组成上的最大区别是.发布:2024/12/25 16:0:1组卷:202引用:5难度:0.3 -
2.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是( )
 发布:2024/12/31 8:0:1组卷:56引用:1难度:0.6
发布:2024/12/31 8:0:1组卷:56引用:1难度:0.6 -
3.甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是( )
 发布:2024/12/31 8:0:1组卷:231引用:2难度:0.5
发布:2024/12/31 8:0:1组卷:231引用:2难度:0.5


